题目内容
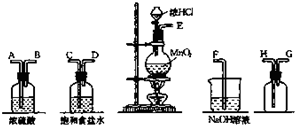
用15.8g KMnO4氧化密度为1.19g·cm-3溶质质量分数为36.5%的HCl溶液。反应方程式如下:
2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O
(1)写出该反应的离子方程式。
(2)求参加反应的盐酸物质的量浓度?
(3)求理论上产生的Cl2在标准状况下的体积为多少?
(4)求有多少克HCl被氧化?
2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O
(1)写出该反应的离子方程式。
(2)求参加反应的盐酸物质的量浓度?
(3)求理论上产生的Cl2在标准状况下的体积为多少?
(4)求有多少克HCl被氧化?
(1)2MnO4-+16H++10Cl-==2Mn2++5Cl2↑+8H2O
(2)11.9mol/L
(3)5.6L
(4)18.25g
(2)11.9mol/L
(3)5.6L
(4)18.25g

练习册系列答案
相关题目