��Ŀ����
��9�֣�ij�о���ѧϰС�����÷�ͭ��ȡCuSO4��
(1) ��ѧ������������ʵ�飺ȡ��6.4gͭ�ķ�ͭ��10ml��18ml��L��1Ũ�������Բ����ƿ�й��ȣ���Ӧ��ϣ��������ƿ�л���ͭƬʣ�ࡣ�������Լ���ѧ�Ļ�ѧ֪ʶ����Ϊ��ƿ�л��н϶������ʣ�ࡣ����Ϊ�����ж��Ƿ���ȷ ���������ǣ�
��
 д����صĻ�ѧ����ʽ��
��
д����صĻ�ѧ����ʽ��
��
(2) ��ͬѧ��Ϊ����Ƶ�ʵ�鷽�����ã����Լ���Ƶ�˼·�ǣ�2Cu+O2==2CuO��CuO+H2SO4
==CuSO4+H2O���Աȼķ�������ͬѧ���ŵ��ǣ�
��
(3) ��ͬѧ�������з�ͭм���ȵ�ϡH2SO4�У�����ͨ�����Ҳ���Ʊ�CuSO4����д����صĻ�ѧ����ʽ�� ��
(1)�ǣ�1�֣������ŷ�Ӧ�Ľ�������Ũ�ȱ�С��ϡ�����ͭ��Ӧ����2�֣�
Cu+2H2SO4(Ũ) CuSO4+SO2+2H2O��2�֣�
CuSO4+SO2+2H2O��2�֣�
(2)���������٣���û����Ⱦ��SO2������2�֣�
(3)2Cu+O2+2H2SO4 2CuSO4 +2H2O��2�֣�
2CuSO4 +2H2O��2�֣�
����������1������ֻ��Ũ������ܺ�ͭ��Ӧ�������ŷ�Ӧ�Ľ�������Ũ�ȱ�С��ϡ�����ͭ��Ӧ����Ӧ�ķ���ʽΪCu+2H2SO4(Ũ) CuSO4+SO2+2H2O��
CuSO4+SO2+2H2O��
��2��Ũ����ֱ�Ӻ�ͭ��Ӧ�������SO2����Ⱦ�����������������Ҳ�ࡣ
��3����Ϊ�ڼ��ȵ������£������ܰ�ͭ��������������ͭ������ͭ�����ᷴӦ����������ͭ������ʽΪ2Cu+O2+2H2SO4 2CuSO4 +2H2O��
2CuSO4 +2H2O��

 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д�
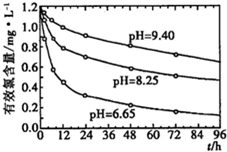


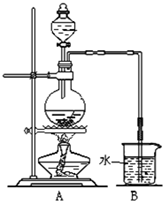 ��ͼ��ij�о���ѧϰС������ʵ������������װ�������ȡ��ˮ���������ʵ�飮
��ͼ��ij�о���ѧϰС������ʵ������������װ�������ȡ��ˮ���������ʵ�飮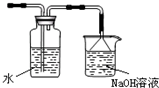 ��
��