题目内容
 一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成nCO2的关系如图.下列有关叙述正确的是( )
一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成nCO2的关系如图.下列有关叙述正确的是( )| A、通入的CO2气体在标准状况下可能大于22.4L | B、A溶液中n(NaOH)=2n(Na2CO3) | C、A溶液中既含Na2CO3,又有NaHCO3 | D、A溶液中一定只有Na2CO3 |
分析:由图象可知,加入盐酸3mol时,开始生成CO2,共消耗1molHCl,发生NaHCO3+HCl=NaCl+CO2↑+H2O,如开始加入盐酸时中发生Na2CO3+HCl=NaCl+NaHCO3,则应消耗1mol盐酸,但至开始生成二氧化碳时消耗3mol盐酸,则说明溶液中含有NaOH和Na2CO3,开始时先后发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3,以此解答该题.
解答:解:由图象可知,加入盐酸3mol时,开始生成CO2,共消耗1molHCl,发生NaHCO3+HCl=NaCl+CO2↑+H2O,如开始加入盐酸时中发生Na2CO3+HCl=NaCl+NaHCO3,则应消耗1mol盐酸,但至开始生成二氧化碳时消耗3mol盐酸,则说明溶液中含有NaOH和Na2CO3,开始时先后发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3,
A.由图象可知生成二氧化碳1mol,则通入的CO2气体在标准状况下应为22.4L,故A错误;
B.由图象可知,反应共生成1mol二氧化碳,则溶液中含有1molNa2CO3,而生成二氧化碳之前分别发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3,共消耗3molHCl,由方程式可知Na2CO3消耗1molHCl,则NaOH消耗2molHCl,则NaOH为2mol,所以n(NaOH)=2n(Na2CO3),故B正确;
C.由以上分析可知A中含有Na2CO3和NaOH,故C错误;
D.A溶液应为Na2CO3和NaOH的混合物,故D错误.
故选B.
A.由图象可知生成二氧化碳1mol,则通入的CO2气体在标准状况下应为22.4L,故A错误;
B.由图象可知,反应共生成1mol二氧化碳,则溶液中含有1molNa2CO3,而生成二氧化碳之前分别发生NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3,共消耗3molHCl,由方程式可知Na2CO3消耗1molHCl,则NaOH消耗2molHCl,则NaOH为2mol,所以n(NaOH)=2n(Na2CO3),故B正确;
C.由以上分析可知A中含有Na2CO3和NaOH,故C错误;
D.A溶液应为Na2CO3和NaOH的混合物,故D错误.
故选B.
点评:本题考查元素化合物、图象数据的处理知识,侧重于学生的分析能力和计算能力的考查,解答此题的易错点是,不能准确理解向碳酸钠溶液中滴加盐酸的反应.是分步进行的,首先发生的是NaOH+HCl=NaCl+H2O,HCl+Na2CO3=NaHCO3+NaCl;进行完全后,再发生:NaHCO3+HCl=NaCl+H2O+CO2↑,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某化学活动小组探究SO2、CO2对品红溶液是否都有漂白作用.
【实验原理】
利用碳酸盐和亚硫酸盐分别与酸反应可以生成CO2和SO2,然后让两种气体直接与品红溶液作用.
【实验装置】
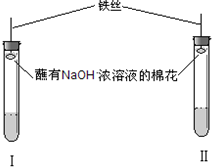
【实验操作和现象】
①请你判断两种气体对品红的漂白性,并将你的结论填写在上表中.
②该实验装置中胶塞上都附着蘸有浓NaOH溶液的棉花,其作用是: .
【问题探究】
他们推测品红可能是一种酸碱指示剂
①你认为他们推测的依据是 .
②请你帮助他们设计实验验证上述推测.实验方案: .
【问题延伸】
某同学将SO2通入酸性高锰酸钾溶液,溶液紫色褪去.他认为该现象表现出SO2的漂白性,你认为正确吗?若不正确,请回答原因;若正确,此空不答 .
【实验原理】
利用碳酸盐和亚硫酸盐分别与酸反应可以生成CO2和SO2,然后让两种气体直接与品红溶液作用.
【实验装置】

【实验操作和现象】
| 实验操作 | 实验现象 | 探究结论 |
| A.取少量品红溶液加入试管Ⅰ中,加入适量碳酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红色 | CO2 |
| B.取少量品红溶液加入试管Ⅱ中,加入适量亚硫酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红,随着反应的进行,颜色又逐渐消失 | SO2 |
②该实验装置中胶塞上都附着蘸有浓NaOH溶液的棉花,其作用是:
【问题探究】
他们推测品红可能是一种酸碱指示剂
①你认为他们推测的依据是
②请你帮助他们设计实验验证上述推测.实验方案:
【问题延伸】
某同学将SO2通入酸性高锰酸钾溶液,溶液紫色褪去.他认为该现象表现出SO2的漂白性,你认为正确吗?若不正确,请回答原因;若正确,此空不答