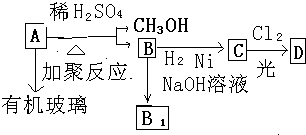
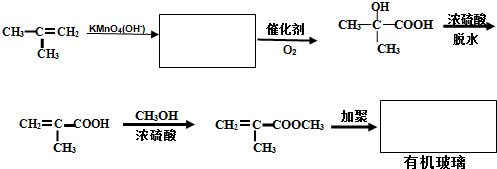
题目内容
16.下列各组物质中,所含分子数相等的是( )| A. | 10g H2和10g O2 | B. | 5.6g N2 (标准状况)和 11g CO2 | ||
| C. | 9g H2O 和0.5mol Br2 | D. | 224mL H2(标准状况)和0.1mol N2 |
分析 根据物质中所含分子数相同,必须所含物质的量相等进行分析.
解答 解:A、等质量的氢气和氧气是氧气的物质的量小,所以分子数不相等,故A错误;
B、5.6g N2 的物质的量为:$\frac{5.6g}{28g/mol}$=0.2mol和11g CO2的物质的量为:$\frac{11g}{44g/mol}$=0.25mol,所以分子数不同,故B错误;
C、9g H2O的物质的量为:$\frac{9g}{18g/mol}$=0.5mol 和0.5mol Br2,物质的量相等所以分子数相同,故C正确;
D、224mL H2(标准状况)的物质的量为:$\frac{224×1{0}^{-3}}{22.4}$=0.01mol与0.1mol N2的物质的量不相等,所以分子数不相同,故D错误;
故选C.
点评 本题主要考查了物质的量的相关计算,侧重考查分析计算能力,难度不大.

练习册系列答案
相关题目
7.下列化学用语使用正确的是( )
| A. | NH4Cl的电子式: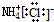 | |
| B. | 氯离子的结构示意图: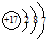 | |
| C. | 乙酸的结构简式:CH3COOH | |
| D. | 硫酸的电离方程式:H2SO4=H++SO42- |
11.下列事实或说法错误的是( )
| A. | 硅是制造太阳能电池的主要材料 | |
| B. | Na、K等金属着火了可用水或泡沫灭火器来灭火 | |
| C. | 漂白粉敞放在空气中容易变质,必须密闭、避光保存 | |
| D. | 铝既能跟稀硫酸、又能与烧碱溶液反应,且都产生氢气 |
8.有关Na2CO3和NaHCO3的叙述中正确的是( )
| A. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同 | |
| B. | Na2CO3比NaHCO3不稳定 | |
| C. | Na2CO3和NaHCO3均可与澄清石灰水反应 | |
| D. | Na2CO3和NaHCO3均可与NaOH溶液反应 |
5.下列仪器能直接用于加热的是( )
| A. | 烧杯 | B. | 量筒 | C. | 坩埚 | D. | 容量瓶 |
6.下列物质所属类别正确的一组是( )
| A. | 混合物:空气、水煤气、碱石灰、水玻璃 | |
| B. | 碱性氧化物:氧化钙、过氧化钠、磁性氧化铁、氧化铝 | |
| C. | 四大基本反应类型:化合、分解、置换、氧化还原 | |
| D. | 正盐:氯化钠、碳酸钠、碳酸氢钠、碱式碳酸铜 |
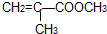 不溶于水,并可以发生以下变化:
不溶于水,并可以发生以下变化: