题目内容
13.若4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol2Fe2O3(s)+3C(s)=3CO2(g)+4Fe (s)△H=+b KJ/mol
C(s)+O2(g)=CO2(g)△H=-c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-($\frac{1}{2}$a-$\frac{1}{2}$b-$\frac{3}{2}$c)KJ/mol.
分析 根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,构造目标热化学方程式.
解答 解:已知:①4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol
②2Fe2O3(s)+3C(s)=3CO2(g)+4Fe (s)△H=+b KJ/mol
③C(s)+O2(g)=CO2(g)△H=-c KJ/mol
由盖斯定律可知,②×$\frac{1}{2}$-③×$\frac{3}{2}$+①×$\frac{1}{2}$得:2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-($\frac{1}{2}$a-$\frac{1}{2}$b-$\frac{3}{2}$c)KJ/mol,
故答案为:2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-($\frac{1}{2}$a-$\frac{1}{2}$b-$\frac{3}{2}$c)KJ/mol.
点评 本题考查利用盖斯定律热书写化学方程式,题目难度不大,注意热化学方程式的书写注意事项.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
12.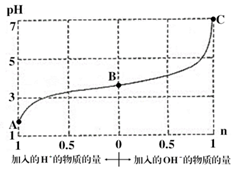 某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1mol•L-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图.下列说法不正确的是( )
某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1mol•L-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图.下列说法不正确的是( )
 某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1mol•L-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图.下列说法不正确的是( )
某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1mol•L-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图.下列说法不正确的是( )| A. | A、B、C三点所表示的溶液中水的电离程度依次增大 | |
| B. | 加入1 mol NaOH后,溶液中c(Na+)=c(R-) | |
| C. | 通入HCl,R-的水解程度增大,HR的电离常数减小 | |
| D. | 未加HCl和NaOH时,溶液中c(R-)>c(Na+)>c(HR) |
4.下列各组溶液,通过溶液的相互滴加顺序不同而不能区别开来的是( )
| A. | 氢氧化钙溶液和碳酸氢钙溶液 | B. | 碳酸钠溶液与稀盐酸 | ||
| C. | 2%的硝酸银溶液和2%的氨水 | D. | 氯化铝溶液和氢氧化钠溶液 |
1.下列有关物质分类的说法中正确的是( )
| A. | 树状分类法是唯一能表示物质分类的方法 | |
| B. | 在物质分类时,一般是先分类,再定标准,这样就不会有误了 | |
| C. | 现有SO42-、N2、CO2、MnO4-,可以按某个标准判断N2与其他三种不同,也按某个标准判断MnO4-与其他三种不同 | |
| D. | 根据组成物质的元素种类是否相同将物质分为纯净物和混合物 |
8.下列反应的离子方程式书写正确的是( )
| A. | 过氧化钠和水反应:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | NH4HCO3溶液中加入过量氢氧化钠溶液:NH4++OH-═NH3•H2O | |
| C. | Ca(ClO)2溶液中通入少量二氧化碳:ClO-+H2O+CO2═HClO+CO32- | |
| D. | 向氯化铝溶液中滴入足量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
18.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,22.4L H2所含原子数为2NA | |
| B. | 100mL 1.0mol•L-1的碳酸钠溶液中,CO32-数目为0.1NA | |
| C. | 1mol S在O2中充分燃烧时,转移的电子数为6NA | |
| D. | 1mol Mg和二氧化碳反应失去电子数为2NA |
5.X、Y、Z、M、W、N 六种元素的原子序数依次增大,其中 X、Y、Z、M、W 为五种短周 期元素.X 原子的最外层电子数等于其电子层数,W 原子核外电子数是 M 原子最外层电 子数的 2 倍,Y、Z、M、W 在周期表中的相对位置如图所示,N 是生活中常见的金属元 素.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | X2Z、YM3、WM4 分子中各原子最外层均为 8 电子稳定结构 | |
| C. | 沸点:X2Z>YM3 热稳定性:XM>X2Z | |
| D. | N 的一种氧化物可用作油漆和涂料 |
3.下列各化合物的命名中正确的是( )
| A. |  1,3,4-三甲苯 1,3,4-三甲苯 | B. |  2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | ||
| C. | CH2=CH-CH=CH2 1,3-二丁烯 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |