题目内容
【题目】以CO2和Na2O2为原料,制取纯净干燥的O2,实验装置如下( )

下列说法正确的是
A. 装置②中试剂为碱石灰
B. 装置③的作用是除去二氧化碳和水
C. .收集氧气应选择装置a
D. 装置②、③之间应增加盛澄清石灰水的洗气瓶,以确认氧气中二氧化碳已经除尽
【答案】D
【解析】
CO2和Na2O2反应生成碳酸钠和氧气,①中盛放的是过氧化钠,②中溶液用于吸收多余的二氧化碳,盛放的是氢氧化钠溶液,③中是浓硫酸,干燥氧气,④是收集氧气的装置,采用向上排空气法收集。
A. ②中溶液用于吸收多余的二氧化碳,则装置②中试剂可以是NaOH溶液,且洗气瓶不能盛放固体除杂试机,A项错误;
B. ③中是浓硫酸,用于干燥氧气,B项错误;
C. ④是收集氧气的装置,氧气密度比空气密度大,采用向上排空气法收集,应该选择装置b,C项错误;
D. 装置②、③之间应增加盛澄清石灰水的洗气瓶,用于检验二氧化碳是否被完全吸收,D项正确;
答案选D。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定,下列实验中用高锰酸钾与浓盐酸反应制备得到氯气,然后再将氯气通入氢氧化钾溶液中与氢氧化铁固体充分反应而制得产品:
(1)制备K2FeO4(夹持装置略)
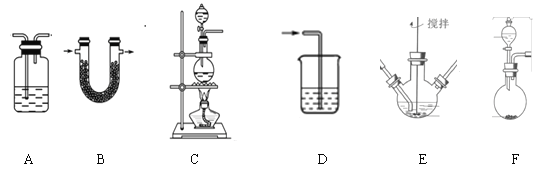
①请写出该过程中制备氯气的离子反应方程式________________(锰被还原为Mn2+)。
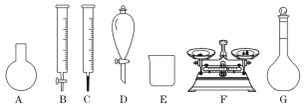
②请根据高铁酸钾制备的原理选择合适的装置,连接顺序为_________→ E →_________。(上述装置不一定全部用到,装置可以重复选用)
③装置E中反应时需进行搅拌,目的是_______________________
④E中得到紫色固体和溶液。E中生成高铁酸钾的反应为______________;反应充分进行后,E中溶液中主要的阴离子为__________________
(2)探究K2FeO4的性质
取E中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否是K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤E中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
②方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________