题目内容
【题目】关于Na2CO3与NaHCO3的性质判断正确的是( )
A.常温下溶解度:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
【答案】D
【解析】
A.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时在水中的溶解性:Na2CO3>NaHCO3,选项A错误;
B.NaHCO3不稳定,加热易分解:2NaHCO3![]() Na2CO3+CO2↑+H2O,碳酸钠受热稳定,选项B错误;
Na2CO3+CO2↑+H2O,碳酸钠受热稳定,选项B错误;
C.分别滴加HCl溶液,碳酸钠溶液中的反应分两步进行:CO32﹣+H+═HCO3﹣,HCO3﹣+H+═H2O+CO2↑,碳酸氢钠溶液中滴加盐酸直接发生反应:HCO3﹣+H+═H2O+CO2↑,所以相同条件下NaHCO3比Na2CO3反应放出气体剧烈,选项C错误;
D.Na2CO3和Ca(OH)2混合后生成CaCO3,发生Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,NaHCO3可与澄清石灰水发生Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O或Ca(OH)2+2NaHCO3═CaCO3↓+Na2CO3+2H2O,选项D正确。
答案选D。

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
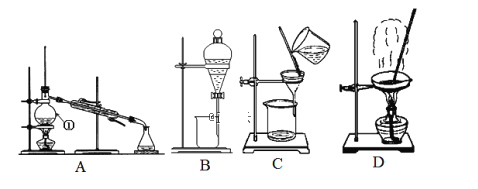
【题目】利用如图装置制取下表中的四种气体(图中夹持仪器已略去;a、b、c表示相应仪器中加入的试剂),能达到实验目的的是( )
选项 | 气体 | a | b | c |
|
A | H2 | 稀硫酸 | Zn | 浓硫酸 | |
B | CO2 | 盐酸 | CaCO3 | 饱和碳酸氢钠溶液 | |
C | NH3 | 浓氨水 | CaO | 浓硫酸 | |
D | Cl2 | 浓盐酸 | MnO2 | 饱和食盐水 |
A.AB.BC.CD.D