题目内容
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)( )
A. NaCl→Na++Cl-
NaCl→Na++Cl-
B. CuCl→Cu2++2Cl-
CuCl→Cu2++2Cl-
C.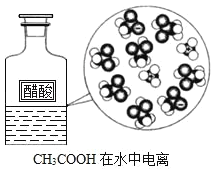 CH3COOHCH3COO-+H+
CH3COOHCH3COO-+H+
D. H2(g)+Cl2(g)→2HCl(g)+183kJ
H2(g)+Cl2(g)→2HCl(g)+183kJ
【答案】B
【解析】
A、NaCl为强电解质,电离方程式为NaCl=Na++Cl-,故A不符合题意;
B、电解氯化铜溶液生成Cu和氯气,电解发生CuCl2![]() Cu+Cl2↑,故B符合题意;
Cu+Cl2↑,故B符合题意;
C、醋酸为弱酸,电离方程式为CH3COOH![]() CH3COO-+H+,故C不符合题意;
CH3COO-+H+,故C不符合题意;
D、焓变等于断裂化学键吸收的能量减去成键释放的能量,则H2(g)+Cl2(g)![]() 2HCl(g)
2HCl(g) ![]() =(436+243-431×2)kJ/mol=-183 kJ/mol,因此H2(g)+Cl2(g)→2HCl(g)+183kJ,故D不符合题意;
=(436+243-431×2)kJ/mol=-183 kJ/mol,因此H2(g)+Cl2(g)→2HCl(g)+183kJ,故D不符合题意;
故选:B。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案【题目】以菱锰矿![]() 主要成分
主要成分![]() ,还含有
,还含有![]() 、
、![]() 等杂质
等杂质![]() 为原料制备二氧化锰的工艺流程如下:
为原料制备二氧化锰的工艺流程如下:
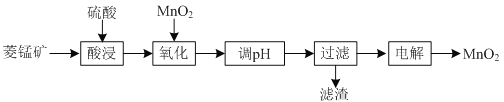
已知部分金属离子开始沉淀及沉淀完全时的pH如下表所示:
金属离子 |
|
|
|
|
开始沉淀时的pH |
|
|
|
|
沉淀完全时的pH |
|
|
|
|
(1)①“酸浸”时![]() 发生反应的离子方程式为________________________________________。
发生反应的离子方程式为________________________________________。
②“酸浸”过程中加入过量硫酸的目的除了加快酸浸的速率、_____________、___________。
③要提高“酸浸”的速率,还可以采取的方法是________________________________________。
(2)“氧化”时发生反应的离子方程式为________________________________________。
(3)“调pH”的目的是除去溶液中的杂质金属离子,“调pH”的范围应为_______________。
(4)当溶液中c(Al3+)≤10-5mol/L时,则认为![]() 沉淀完全,则
沉淀完全,则![]() ______________。
______________。