题目内容
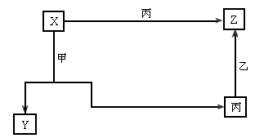
三种常见单质甲、乙、丙,三种常见的化合物X、Y、Z,它们在一定条件下有如图的相互转化关系:
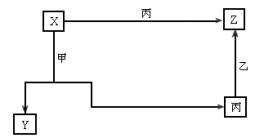
试通过分析确定化学式:X_________、Y_________、Z__________、甲________、乙_________、丙___________,相关的化学反应方程式为_________________。
解析:
精析 此题是一道涉及元素化合物知识的框图题,题目中没有给出明显的突破口和切入点。因此,惟一可以着手的地方就是它们之间的转化关系。 转化关系“乙+丙→Z”说明Z是由乙、丙两种元素组成;又转化关系“X+丙→Z”说明X也是由乙、丙两种元素组成的。显然,乙元素或丙元素中的一种在X、Z中呈现不同的化合价,也就是说该元素具有变价的特点。那么,可考虑的元素范围为“C、N、P、Cl、Na、Fe”,且X属于氧化物或卤化物的可能性较大。再从“X+甲→Y+丙”这个置换反应来看,甲单质比丙单质活泼(甲比丙金属活动性强或非金属活动性强)。且Y由甲、乙两种元素组成。 若X、Y、Z为氧化物,则甲是一个能把氧化物还原成单质而把自己变成氧化物的物质。X、Z是同一元素形成的价态不同的氧化物,且其中的高价氧化物能与该元素的单质反应生成低价氧化物。由此,可确定甲为Mg,乙为O2,符合题意的变价元素丙是“C”。即:甲为Mg,丙为C,乙为O2,X为CO2,Y为MgO,Z为CO。相关反应为2C+O2══2CO;CO2+C══2CO;CO2+2Mg══C+2MgO 若X、Y、z为卤化物(氯化物或溴化物),则甲是一个能把卤化物氧化成单质而把自己变成卤化物的物质。X、Z是同一元素形成的价态不同的卤化物,且其中的高价卤化物能与该元素的单质反应生成低价卤化物。由此,可确定甲是一活泼性较强的卤素单质——Cl2,丙为Br2(丙不能考虑为I2,因为Fel2和I2不反应),符合题意的变价元素乙是“Fe”。即:甲为Cl2,丙为Br2,乙为Fe,X为FeBr2,Y为FeCl3,Z为FeBr3。相关反应为:2FeBr2+3Cl2══2FeCl3+2Br2;2Fe+3Br2══2FeBr3;2FeBr2+Br2══2FeBr3 答案 CO2 MgO CO Mg O C 2C+O2══2CO;CO2+C══2CO;CO2+2Mg══C+2MgO FeBr2 FeCl3 FeBr3 Cl2 Fe Br2 2FeBr2+3Cl2══2FeCl3+2Br2;2Fe+3Br2══2FeBr3;2FeBr2+Br2══2FeBr3
|

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案 甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体;它们之间的转化关系如图所示.请填写下列空白:
甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体;它们之间的转化关系如图所示.请填写下列空白: