题目内容
13.下列说法不正确的是( )| A. | 最外层电子数为次外层电子数一半的短周期主族元素只有Li、Si两种元素 | |
| B. | 元素周期表中从ⅢB族到ⅡB族之间10个纵行的元素都是金属元素 | |
| C. | 同周期第ⅡA族与第ⅢA族元素的原子序数相差1或11或25 | |
| D. | 若主族元素的族序数为a,周期数为b,当$\frac{a}{b}$<1,该元素为非金属元素 |
分析 A、两个电子层最外层电子数为次外层电子数一半的短周期主族元素Li,三个电子层最外层电子数为次外层电子数一半的短周期主族元Si;
B、过渡元素都是金属元素;
C、根据元素所在周期表中的位置判断;
D.元素Li族序数为1,周期数为2,当$\frac{a}{b}$=$\frac{1}{2}$<1,是金属元素.
解答 解:A、两个电子层最外层电子数为次外层电子数一半的短周期主族元素Li,三个电子层最外层电子数为次外层电子数一半的短周期主族元Si,所以最外层电子数为次外层电子数一半的短周期主族元素只有Li、Si两种元素,故A正确;
B、过渡元素都是金属元素,非金属元素都处于主族与0族中,故B正确;
C.第二、三周期的第ⅡA族和第ⅢA族元素的原子序数相差1,第四、五周期的第ⅡA族和第ⅢA族元素的原子序数相差11,第六、七周期的第ⅡA族和第ⅢA族元素的原子序数相差25,故C正确;
D.元素Li族序数为1,周期数为2,当$\frac{a}{b}$=$\frac{1}{2}$<1,是金属元素,故D错误.
故选D.
点评 本题考查原子结构、元素周期表、元素周期律等,难度较小,注意D得用元素的特殊性来解答.

练习册系列答案
相关题目
2.下表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
(1)F元素在周期表中的位置是第三周期第ⅢA族.
(2)写出C元素氢化物的电子式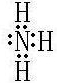 .
.
(3)C和D两种元素氢化物的稳定性更强的是H2O>NH3(填物质的化学式)
(4)用电子式表示离子化合物EG的形成过程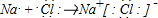 .
.
| A | |||||||
| B | C | D | |||||
| E | F | G | |||||
(2)写出C元素氢化物的电子式
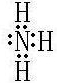 .
.(3)C和D两种元素氢化物的稳定性更强的是H2O>NH3(填物质的化学式)
(4)用电子式表示离子化合物EG的形成过程
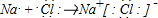 .
.
3.下列表示对应化学反应的离子方程式正确的是( )
| A. | 工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- | |
| B. | 碳酸钠的水解:CO32-+2H2O═H2CO3+2OH- | |
| C. | 硫酸铝溶液中滴加过量浓氨水:Al3++4 NH3•H2O═AlO${\;}_{2}^{-}$+4NH4++2H2O | |
| D. | 用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
18.质量相同的下列烃,完全燃烧,耗氧量最多的是( )
| A. | C2H6 | B. | C4H6 | C. | C5H10 | D. | CH4 |
5.下列装置能组成原电池产生电流的是( )
| A. |  | B. |  | C. |  | D. |  |
3.下列各组顺序的排列不正确的是( )
| A. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 | B. | 热稳定性:HF>HCl>H2S>PH3 | ||
| C. | 微粒半径:Na+>Mg2+>Al3+>F- | D. | 熔点:SiO2>NaCl>I2>CO2 |