题目内容
下列说法中错误的是
A.10 g 98%硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的
B.制成0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L(标准状况下)
C.0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.从1 L 1 mol/L的NaCl溶液中取出500 mL,其浓度是0.5 mol/L
【答案】
D
【解析】
试题分析:根据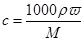 可知,98%硫酸(密度为1.84 g/cm3)的物质的量浓度是18.4mol/L,A正确;0.5 L 10 mol/L的盐酸中氯化氢的物质的量是5mol,标准状况下的体积是112L,B正确;0.5 L 2 mol/L BaCl2溶液中氯化钡的物质的量是1mol,所以离子的总的物质的量是3mol,C正确;D不正确,因为溶液是均一稳定的,所以浓度是不变的,D不正确,答案选D。
可知,98%硫酸(密度为1.84 g/cm3)的物质的量浓度是18.4mol/L,A正确;0.5 L 10 mol/L的盐酸中氯化氢的物质的量是5mol,标准状况下的体积是112L,B正确;0.5 L 2 mol/L BaCl2溶液中氯化钡的物质的量是1mol,所以离子的总的物质的量是3mol,C正确;D不正确,因为溶液是均一稳定的,所以浓度是不变的,D不正确,答案选D。
考点:考查物质的量浓度的有关计算与判断
点评:在判断溶液中离子浓度大小时,需要注意分析提供该离子的电解质的组成特点。而在计算离子的数目时,还需要注意溶液的体积。另外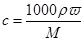 在浓度的计算中也经常用到,需要熟练掌握。
在浓度的计算中也经常用到,需要熟练掌握。

练习册系列答案
相关题目
下列说法中错误的是( )
| A、NH3比PH3稳定 | B、S2- 的离子半径比Cl-离子半径大 | C、第3周期元素中,金属性最强的是Na,非金属性最强的是Cl | D、第ⅡA元素中,Be是化学性质最活泼的金属元素 |
关于甲醛的下列说法中错误的是( )
| A、甲醛是最简单的一种醛,易溶解于水 | B、甲醛是一种无色、有刺激性气味的气体 | C、35%-40%甲醛的水溶液被称之为福尔马林(formalin) | D、福尔马林有杀菌、防腐性能,所以市场上可原来浸泡海产品等 |
 某同学在实验室进行了如图所示的实验,下列说法中错误的是( )
某同学在实验室进行了如图所示的实验,下列说法中错误的是( )