题目内容
V L氯化镁溶液和V L氯化钠溶液混合后,Cl-物质的量浓度为0.3mol/L,原氯化镁溶液和氯化钠溶液的浓度可能是( )
| A、均为0.3mol/L |
| B、分别为0.1mol/L和0.4mol/L |
| C、分别为0.1mol/L和0.2mol/L |
| D、均为0.6mol/L |
考点:物质的量浓度的相关计算
专题:
分析:1mol氯化镁能电离出2mol氯离子,1mol氯化钠能电离出1mol氯离子,根据n=c×v设氯化镁溶液的物质的量浓度为xmol/L,氯化钠的物质的量浓度为ymol/L,求出氯化镁和氯化钠所含的氯离子的物质的量,再根据Cl-物质的量浓度为0.3mol/L和溶液的总体积2V求出氯离子的物质的量,两者相等,据此分析解答.
解答:
解:设氯化镁溶液的物质的量浓度为xmol/L,氯化钠的物质的量浓度为ymol/L,
VL氯化镁溶液中n(Cl-)=2×xmol/L×VL=2xVmol,VL氯化钠溶液中n(Cl-)=ymol/L×VL=yVmol,溶液中含有的氯离子的物质的量为2xVmol+yVmol=(2xV+yV)mol,
Cl-物质的量浓度为0.3mol/L,总体积为2V,溶液中含有的氯离子的物质的量为:0.3mol/L×2VL=0.6Vmol,则2xV+yV=0.6V,2x+y=0.6,
A.2x+y=2×0.3+0.3=0.9≠0.6,故A错误;
B.2x+y=2×0.1+0.3=0.6,故B正确;
C.2x+y=2×0.1+0.2=0.4≠0.6,故C错误;
D.2x+y=2×0.6+0.6=1.8≠0.6,故D错误;
故选B.
VL氯化镁溶液中n(Cl-)=2×xmol/L×VL=2xVmol,VL氯化钠溶液中n(Cl-)=ymol/L×VL=yVmol,溶液中含有的氯离子的物质的量为2xVmol+yVmol=(2xV+yV)mol,
Cl-物质的量浓度为0.3mol/L,总体积为2V,溶液中含有的氯离子的物质的量为:0.3mol/L×2VL=0.6Vmol,则2xV+yV=0.6V,2x+y=0.6,
A.2x+y=2×0.3+0.3=0.9≠0.6,故A错误;
B.2x+y=2×0.1+0.3=0.6,故B正确;
C.2x+y=2×0.1+0.2=0.4≠0.6,故C错误;
D.2x+y=2×0.6+0.6=1.8≠0.6,故D错误;
故选B.
点评:本题考查了物质的量的简单计算,题目难度中等,可以根据混合物的各成分氯离子的物质的量与Cl-物质的量浓度为0.3mol/L关系求解,本题侧重对学生灵活运用基础知识解决实际问题的能力的培养.

练习册系列答案
相关题目
下列反应中氯元素被氧化的是( )
| A、5Cl2+I2+6H2O═10HCl+2HIO3 | ||||
| B、2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | ||||
| C、MnO2+4HCl═MnCl2+2H2O+Cl2↑ | ||||
D、2NaCl+2H2O
|
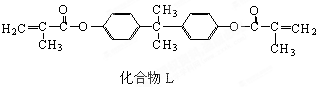 化合物L是一种能使人及动物的内分泌系统发生紊乱导致生育及繁殖异常的环境激素,它在一定条件下水解可生成双酚A和有机酸M.下列关于L、双酚A和M的叙述中正确的是( )
化合物L是一种能使人及动物的内分泌系统发生紊乱导致生育及繁殖异常的环境激素,它在一定条件下水解可生成双酚A和有机酸M.下列关于L、双酚A和M的叙述中正确的是( )| A、1mol L水解可以消耗2molNaOH |
| B、双酚A与苯酚互为同系物 |
| C、与M含相同官能团的同分异构体还有2种 |
| D、L、双酚A和M 均能与溴水发生加成反应 |
下列各组气体通常情况下能大量共存,并且既能用浓硫酸干燥,又能用无水氯化钙干燥的是( )
| A、SO2、O2、HI |
| B、NH3、O2、N2 |
| C、NH3、CO2、HCl |
| D、H2、Cl2、O2 |
有“智力元素”之称的是( )
| A、Ca | B、O | C、I | D、F |
下列有关实验原理或操作正确的是( )
| A、室温下向苯和苯酚的混合溶液中加入浓溴水,充分反应后过滤,以除去苯中少量苯酚 |
| B、酸碱中和滴定前,滴定管用蒸馏水洗涤后用待装溶液润洗 |
C、 用如图所示装置检验有乙烯生成 |
D、 用如图所示装置收集SO2 |
下列叙述正确的是( )
| A、Na2O与Na2O2都能和水反应生成碱,它们是碱性氧化物 |
| B、Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀 |
| C、Na2O2应保存于密封、干燥带玻璃塞的广口瓶中 |
| D、Na2O2可作供氧剂,而Na2O不行 |
某物质经鉴定只含一种元素,则该物质不可能是( )
| A、一种混合物 | B、一种化合物 |
| C、一种单质 | D、是纯净物 |