题目内容
(9分)已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:

(1)若条件①为点燃,目前60%的B都是从海水中提取的,气体D可以使湿润的红色石蕊试纸变蓝,写出C与H2O反应的化学方程式_____________。将气体D作为燃料电池的燃料源可以制成D—空气燃料电池系统,总反应式为:D+O2 A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________。
A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________。
(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,则C为____________(写化学式)。
(3)若条件①为常温,B和D为同种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的稀溶液反应的离子方程式:_________________________________。
已知常温下1molC与H2O反应生成气体D和E溶液放出46kJ热量,写出C与水反应生成D和E的热化学方程式:________________________。
(9分)(1) Mg3N2+6H2O=3Mg(OH)2↓+ 2NH3↑ (2分) ;2NH3 - 6e-+6OH-=N2+6H2O (2分)
(2) Al2S3(1分;(3) Fe + 4H+ + NO3—=Fe3+ + NO↑+ 2H2O; (2分)
3NO2(g)+ H2O (l)=2HNO3(aq)+ NO(g) △H=-138KJ/mol (2分)
【解析】
试题分析:根据物质的转化、性质可知:A是N2;B是Mg;C是Mg3N2;D是NH3;E是Mg(OH)2。(1)C与H2O反应的化学方程式是Mg3N2+6H2O=3Mg(OH)2↓+ 2NH3↑;将气体NH3作为燃料电池的燃料源可以制成D—空气燃料电池系统,总反应式为:4NH3+3O2==2N2+6H2O,此碱性燃料电池的负极材料是NH3,电极反应式是2NH3 - 6e-+6OH-=N2+6H2O;(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,则A是S;B是Al,或A是Al;B是S,C为Al2S3。D是H2S;E是Al(OH)3。(3)若条件①为常温,B和D为同种无色气体,常温下E的浓溶液可以使Fe钝化,则A是O2;B是NO;C是NO2;D是NO,E是HNO3。Fe是变价金属,当Fe粉少量时与HNO3的稀溶液反应变为Fe3+。该反应的离子方程式Fe + 4H+ + NO3—=Fe3+ + NO↑+ 2H2O。在常温下1molC与H2O反应生成气体D和E溶液放出46kJ热量,则C与水反应生成D和E的热化学方程式是3NO2(g)+ H2O (l)=2HNO3(aq)+ NO(g) △H=-138KJ/mol。
考点:考查元素的单质及化合物的推断、化学方程式、离子方程式、热化学方程式、燃料电池的电极反应式的书写的知识。

中学实验室为完成下列实验通常选择的装置正确的是
A | B | C | D | |
实验 | 用CCl4萃取 溴水中的溴 | 从NaCl与I2的混合物中回收I2 | 制备与收集二氧化硫 | 制备乙酸丁酯 |
装置 |
|
|
|
|
 )及其衍生物冬青油(结构简式:
)及其衍生物冬青油(结构简式: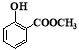 )和阿司匹林(结构简式:
)和阿司匹林(结构简式: )都是常用的药物。
)都是常用的药物。







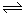 CO2+H2(g)
CO2+H2(g)