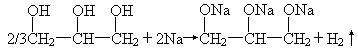题目内容
现将甲醇、乙二醇、丙三醇分别与足量的金属钠反应,若要使三者生成的H2体积相等,则使用的三种醇的物质的量之比为________.
答案:6∶3∶2
解析:
提示:
解析:
|
【答案】6∶3∶2 【解析】醇分子中的 三种醇与金属钠反应的化学方程式分别为: 2CH3 HO 设生成的H2均为1mol,根据上面的反应方程式,可计算出三种醇的物质的量之比为6∶3∶2. |
提示:
|
【方法提炼】 有机物分子中能与金属钠发生置换反应的活泼H除了羟基氢外,还有羧基氢,其反应的比例也为 |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 OH上的H原子较活泼,可与活泼金属(如钠)发生置换反应.
OH上的H原子较活泼,可与活泼金属(如钠)发生置换反应.