题目内容
15.常温下,下列有关试剂保存正确的是( )| A. | 用无色试剂瓶盛放浓硝酸 | B. | 用铁质容器盛放浓硫酸 | ||
| C. | 用玻璃试剂瓶盛放氢氟酸 | D. | 用带橡胶塞的试剂瓶盛放苯 |
分析 A.浓硝酸见光易分解;
B.常温下,浓硫酸能使铁、铝发生钝化,在金属表面形成致密的氧化膜;
C.二氧化硅能和氢氟酸反应;
D.苯是橡胶的良溶剂,会使橡胶溶解.
解答 解:A.浓硝酸见光易分解,须存放在棕色试剂瓶中,故A错误;
B.常温下,浓硫酸能使铁、铝发生钝化,故可用铁质容器盛放浓硫酸,故B正确;
C.二氧化硅能和氢氟酸反应,所以氢氟酸不能盛放在玻璃试剂瓶中,故C错误;
D.苯是橡胶的良溶剂,会使橡胶溶解,所以不能用带橡胶塞的试剂瓶盛放苯,故D错误;
故选B.
点评 本题考查化学试剂的存放,难度不大.了解所存放物质的特性时解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 0.1mol苯分子中含有双键数为0.3NA | |
| B. | 1L1mol•L-1碳酸钠溶液中阴离子的数目大于NA | |
| C. | 标准状况下,22.4L乙烷中共含有分子数为NA | |
| D. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,转移的电子的数目为0.92NA |
3.下列有关图示分析正确的是( )
| A. |  如图所示,集气瓶内充满Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,并可能充满集气瓶 | |
| B. | 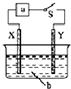 如图所示,X为铁棒,Y为铜棒,a为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入a | |
| C. | 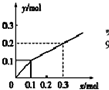 Pt为电极,电解含0.10 mol M+和0.1 mol N3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图,离子氧化能力M+>N3+>H+ | |
| D. | 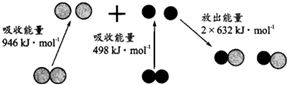 如图为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N≡N的键能为946kJ/mol,热化学方程式为:N2(g)+O2(g)═2NO(g)△H=-180 kJ/mol |
20.我省近年来以铁矿石为原料的产业发展迅猛,下列有关说法正确的是( )
| A. | 以焦炭和铁矿石为原料炼铁的原理是用焦炭直接还原化合态的铁 | |
| B. | 据报道,庐江磁性材料产生“磁”力无穷,磁性氧化铁的化学式是Fe2O3 | |
| C. | 为证明某铁矿石中存在铁离子,可将铁矿石溶于硝酸后,再加KSCN溶液 | |
| D. | 利用铁矿石制得的能除去污水中的,可知相同条件下,Ksp(FeS)>Ksp(HgS) |
7.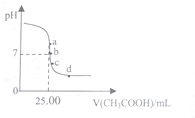 室温下,向25.00mL0.1000mol•L-1的NaOH溶液中逐滴滴入0.1000mol•L-1CH3COOH溶液,PH曲线变化如图所示,则下列说法一定正确的是( )
室温下,向25.00mL0.1000mol•L-1的NaOH溶液中逐滴滴入0.1000mol•L-1CH3COOH溶液,PH曲线变化如图所示,则下列说法一定正确的是( )
 室温下,向25.00mL0.1000mol•L-1的NaOH溶液中逐滴滴入0.1000mol•L-1CH3COOH溶液,PH曲线变化如图所示,则下列说法一定正确的是( )
室温下,向25.00mL0.1000mol•L-1的NaOH溶液中逐滴滴入0.1000mol•L-1CH3COOH溶液,PH曲线变化如图所示,则下列说法一定正确的是( )| A. | a点:c(CH3COONa)=0.1000 mol•L-1 | B. | b点:c(CH3COONa)=c(CH3COOH) | ||
| C. | c点:c(H+)=c(CH3COO-)+c(CH3COOH) | D. | d点:c(Na+)<c(CH3COO-)+c(CH3COOH) |
11.近年流行喝苹果醋.苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等作用的保健食品.苹果酸(α羟基丁二酸)是这种饮料的主要酸性物质,其结构如图所示: 下列相关说法正确的是( )
下列相关说法正确的是( )
 下列相关说法正确的是( )
下列相关说法正确的是( )| A. | 苹果酸在一定条件下能催化氧化生成醛 | |
| B. | 苹果酸在一定条件下能发生取代和消去反应 | |
| C. | 苹果酸在一定条件下能发生加聚反应生成高分子化合物 | |
| D. | 1 mol苹果酸与Na2CO3溶液反应最多消耗1 mol Na2CO3 |