题目内容
用![]() 和HCl溶液作试剂,除去NaCl溶液中含有的少量Ca2+和
和HCl溶液作试剂,除去NaCl溶液中含有的少量Ca2+和![]() 。每种试剂不得重复用两次。提纯过的溶液中除了Na+、Cl-、H+和OH-外,不得遗留任何其他离子。
。每种试剂不得重复用两次。提纯过的溶液中除了Na+、Cl-、H+和OH-外,不得遗留任何其他离子。
(1)写出加入试剂的顺序。
(2)写出各步反应的离子方程式。
答案:
解析:
解析:
由于反应终点较难控制,要使离子完全沉淀,所加试剂必须是过量的,而由过量试剂引入新的杂质亦必须除尽。此题不能回答为,加入适量Na2CO3溶液,使Ca2+生成CaCO3沉淀,过滤除去,再加入适量BaCl2溶液使SO42-生成BaSO4沉淀,过滤除去,在实验中控制适量很困难,为使杂质完全除去,都加入过量的沉淀试剂。此题中,先加过量BaCl2溶液,溶液中有多余的Ba2+,可在下一步加Na2CO3溶液除Ca2+时一并除去(生成BaCO3沉淀),此时又引入过量的Na2CO3可用HCl处理除去。此题允许溶液有H+存在,故不必考虑除去多余的HCl,若不允许H+过量,可将溶液蒸发干,将HCl驱除,剩余纯的NaCl,再溶解于水,即得到不含HCl的NaCl溶液 答案:(1)BaCl2、Na2CO3、HCl溶液; (2)Ba2++SO42-══BaSO4↓; Ca2++CO32-══CaCO3↓; Ba2++CO33-══BaCO3↓ CO32-+2H+══CO2↓+H2O
|

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
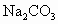 、
、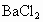 和HCl溶液作试剂,除去NaCl溶液中含有的少量
和HCl溶液作试剂,除去NaCl溶液中含有的少量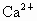 和
和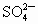 .每种试剂不得重
.每种试剂不得重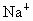 、
、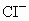 、
、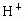 和
和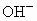 离子外,不得遗留任何其他离子.
离子外,不得遗留任何其他离子.