题目内容
下面有关合金说法正确的是( )
| A、现代使用最广泛的合金是铝合金 |
| B、我国使用最早的合金是铁合金 |
| C、合金的熔点比各组分单质大 |
| D、合金的硬度比各组分单质大 |
考点:金属与合金在性能上的主要差异
专题:几种重要的金属及其化合物
分析:A、现代使用最广泛的合金是铁合金;
B、我国使用最早的合金是铜合金,即青铜;
C、合金的熔点比成分金属低;
D、合金的硬度比成分金属大;
B、我国使用最早的合金是铜合金,即青铜;
C、合金的熔点比成分金属低;
D、合金的硬度比成分金属大;
解答:
解:A、铁合金是现代使用最广泛的合金,故A错误;
B、青铜是我国使用最早的合金,故B错误;
C、合金的熔点比各组分单质低,故C错误;
D、合金的硬度比各组分单质大,故D正确;
故选D.
B、青铜是我国使用最早的合金,故B错误;
C、合金的熔点比各组分单质低,故C错误;
D、合金的硬度比各组分单质大,故D正确;
故选D.
点评:本题主要考查金属及合金的知识,注意使用合金的时间与冶炼技术有关,题目难度不大.

练习册系列答案
相关题目
有关常温下pH均为11的氨水和Ba(OH)2溶液的说法正确的是( )
| A、两溶液中,由水电离出的氢氧根离子浓度均为1×10-11mol/L |
| B、分别加水稀释100倍后,两种溶液的pH均变为9 |
| C、氨水中的c(NH+)和Ba(OH)2溶液中的c(Ba2+)相等 |
| D、分别加入等量的pH为1的硫酸,二者的导电能力均减小 |
有机物的结构简式可以用“键线式”表示,其中线表示键,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来.已知利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应为: (反应吸热),下列叙述中错误的是( )
(反应吸热),下列叙述中错误的是( )
 (反应吸热),下列叙述中错误的是( )
(反应吸热),下列叙述中错误的是( )| A、NBD和Q互为同分异构体 |
| B、NBD的同分异构体可以是芳香烃 |
| C、Q的一氯代物只有3种 |
| D、Q可使溴水褪色 |
下列离子方程式正确的是( )
| A、Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- |
| B、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
| C、明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
| D、双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O |
除去CO2的SO2不能选用的试剂是( )
| A、NaOH溶液反应 |
| B、高锰酸钾溶液 |
| C、溴水 |
| D、饱和的 NaHCO3溶液 |
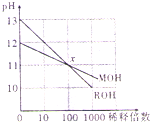 常温下,两种一元碱MOH和ROH的溶液分别加水稀释时,pH变化如图所示.下列有关说法正确的是( )
常温下,两种一元碱MOH和ROH的溶液分别加水稀释时,pH变化如图所示.下列有关说法正确的是( )| A、RCl溶液pH<7 |
| B、稀释前,c(ROH)=10c(MOH) |
| C、在x点,c(M+)=c(R+) |
| D、等体积的pH=12的MOH溶液和pH=2的盐酸混合,c(M+)=c(Cl-) |
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,其中可以实现实验目的是( )
| A、测所得溶液的pH |
| B、取溶液少量,向其中滴入酚酞观察溶液是否变红 |
| C、取溶液少量,向其中加入盐酸观察是否有气泡产生 |
| D、取溶液少量,向其中加入CuSO4溶液,观察是否有沉淀产生 |
将四个分别盛有足量硫酸铜溶液、氯化铜溶液、氢氧化钾溶液、氯化钠溶液的电解槽串联,用惰性电极电解一段时间后四个电解槽两极共产生气体在同温同压下的体积之比为( )
| A、1:1:2:2 |
| B、1:2:3:4 |
| C、1:2:2:1 |
| D、2:2:2:3 |
如表代表周期表中的几种短周期元素,下列说法中正确的是( )


| A、C、D的氢化物沸点D比C高 |
| B、第一电离能A、B、C依此增大 |
| C、A、B、C中电负性最大的A |
| D、五种元素中,最高价氧化物对应的水化物酸性最强的是D |