题目内容
【题目】伞形酮可用作荧光指示剂和酸碱指示剂,其合成方法为: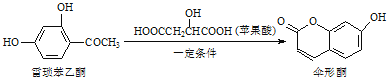 ,下列有关这三种物质的说法正确的是( )
,下列有关这三种物质的说法正确的是( )
A. 每个雷琐苯乙酮、苹果酸和伞形酮分子中均含有1个手性碳原子
B. 雷琐苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应
C. 1 mol雷琐苯乙酮跟足量H2反应,最多消耗3molH2
D. 1 mol伞形酮与足量NaOH溶液反应,最多消耗3molNaOH
【答案】BD
【解析】
A.若碳原子连有不同的四个原子或基团,则具有手性,只有苹果酸中含有手性碳原子;
B.根据含酚羟基的物质遇氯化铁溶液发生显色反应分析;
C.雷琐苯乙酮含有苯环、羰基,均能与氢气发生加成反应;
D.酚羟基、酯基都能与NaOH溶液反应。
A.若碳原子连有不同的四个原子或基团,则具有手性,显然只有苹果酸中与﹣OH相连的碳原子为手性碳原子,A错误;
B.雷琐苯乙酮和伞形酮都含有酚羟基,则都能跟FeCl3溶液发生显色反应,B正确;
C.雷琐苯乙酮含有苯环、羰基,均能与氢气发生加成反应,1mol雷琐苯乙酮跟足量H2反应,最多消耗4mol H2,C错误;
D.酚羟基、酯基都能与NaOH溶液反应,因为该酯基为酚酯基,则1mol伞形酮与足量NaOH溶液反应,最多消耗3molNaOH,D正确;
故合理选项是BD。

【题目】在2 L的密闭容器内,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=___________________________。已知:K300℃>K350℃,则该反应是______热反应。
(2)下图表示NO2变化的曲线是____。用O2表示从0~2 s内该反应的平均速率v=_________。

(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂