题目内容
(6分)A、B、C、D、E均为中学化学常见物质,A是短周期原子半径最大的元素(稀有气体除外)构成的单质,E既可溶于盐酸又可溶于NaOH溶液,它们之间的反应关系如图所示:

(1)E溶于NaOH溶液的离子方程式为 ;
(2)工业上冶炼A的化学反应方程式为 ;
(3)气体C在使用前需要检验纯度,操作方法是 。
(1)Al(OH) 3 +OH-= AlO2-+2H2O;(2分);2NaCl(熔融) 2Na + Cl2↑;(3分)收集一试管气体,用拇指堵住试管口移近火焰,松开拇指点燃后,若发出轻微的响声,证明气体纯净。
2Na + Cl2↑;(3分)收集一试管气体,用拇指堵住试管口移近火焰,松开拇指点燃后,若发出轻微的响声,证明气体纯净。
【解析】
试题分析:根据题意可知A是Na;B是含有Al元素的盐溶液,C是H2;D是NaAlO2溶液;E是Al(OH) 3。(1)E :Al(OH) 3溶于NaOH溶液的离子方程式为Al(OH) 3 +OH-= AlO2-+2H2O;(2)由于Na是特别活泼的金属,用一般的还原剂不能还原出来,所以在工业上冶炼Na是用电解熔融的NaCl的方法来制取的,化学反应方程式为2NaCl(熔融) 2Na + Cl2↑;(3)由于H2是可燃性气体,若点燃混合气体,在短时间内会放出大量的热,使气体的体积急剧膨胀发生爆炸,所以C在使用前需要检验纯度,操作方法是收集一试管气体,用拇指堵住试管口移近火焰,松开拇指点燃后,若发出轻微的响声,证明气体纯净。
2Na + Cl2↑;(3)由于H2是可燃性气体,若点燃混合气体,在短时间内会放出大量的热,使气体的体积急剧膨胀发生爆炸,所以C在使用前需要检验纯度,操作方法是收集一试管气体,用拇指堵住试管口移近火焰,松开拇指点燃后,若发出轻微的响声,证明气体纯净。
考点:考查元素及化合物的推断、氢氧化铝的的两性、Na的冶炼方法、可燃性气体验纯的方法的知识。

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
 ,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为:
,向次氯酸钠溶液中通入少量二氧化碳的离子方程式为: 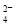 完全沉淀:
完全沉淀: +Al3++2SO
+Al3++2SO