题目内容
25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH—)的变化关系如图所示,则
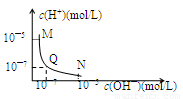
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO―)>c(Na+)
C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
D.M点和N点所示溶液中H2O的电离程度相同
【答案】
D
【解析】
试题分析:A.由于醋酸是弱酸,电离程度很小,离子浓度也较小,M点溶液的导电能力最弱,故A错误;B.N点所示溶液为碱性,根据溶液电荷守恒易判断出此时c(Na+)>c(CH3COO﹣),故B错误;D.由于M点的H+浓度等于N点的OH﹣浓度,对水的电离程度抑制能力相同,所以两点水电离程度相同,故D正确;C.Q点的pOH=pH,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性.则所加NaOH溶液体积略小于醋酸溶液的体积,故C错误,故选D。
考点:本题考查酸碱中和的定性判断和计算,侧重于弱电解质的电离的考查,注意弱电解质的电离特点,把握pOH的含义,题目难度中等。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、101 kPa时,1 mol H2燃烧生成水蒸气放出的热量叫做H2的燃烧热 | B、0.25molNa2O2中含有的阴离子数约为0.25×6.02×1023 | C、向0.2 mol?L-1NaHCO3溶液中加入等体积0.1 mol?L-1NaOH溶液,反应后溶液中:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | D、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
 CO(g)+H2(g)△H=+131kJ?mol-1
CO(g)+H2(g)△H=+131kJ?mol-1 CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)
CH3OH(g) 据研究,给合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示) 2Cu+CO2
2Cu+CO2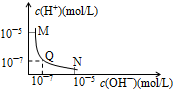 25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH-)的变化关系如图所示,则( )
25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH-)的变化关系如图所示,则( ) 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围: