��Ŀ����
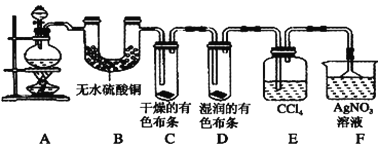
����Ŀ����.ijУ��ѧʵ����ȤС��Ϊ����֤��ʵ�����Ʊ�Cl2�Ĺ�������ˮ������HCl�ӷ�������ͬʱ֤��Cl2��ijЩ���ʣ���ͬѧ�������ͼ��ʾ��ʵ��װ��(֧���õ�����̨ʡ��)���밴Ҫ��ش��������⡣
(1) ʵ�����Ʊ�Cl2���õĻ�ѧҩƷ��________��
д���÷�Ӧ�����ӷ���ʽ�����õ����ű�ʾ����ת�����_____________________ ���˷�Ӧ��ÿת��0.8mol���ӣ�����Hcl____mol
(2)��װ��B��������_______
��װ��C��D���ֵIJ�ͬ����˵����������___
��װ��E��������_______
(3)��ͬѧ��Ϊ��ͬѧ��ʵ����ȱ�ݣ�����ȷ������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�Ϊ��ȷ��ʵ����۵Ŀɿ��ԣ�֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֣���ͬѧ���Ӧ����װ��___��___֮��(��װ����ĸ���)����һ��װ�ã�������װ��������Լ�����Ϊ___(����ĸ���)��
A.ʪ��ĵ⻯�ص�����ֽ B.Ũ���� C.ʪ��ĺ�ɫ���� D.����ʳ��ˮ
��.���ֹ�������ˮ������ɱ����Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��Ư���dz��õ���������
�ٹ�ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]��ȡƯ�ۣ���ѧ��Ӧ����ʽΪ��_____________��
��Ư�۵���Ч�ɷ���________________________��
��Ư������ˮ���ܿ����е�CO2���ã���������Ư�ס�ɱ�����õĴ����ᣬ��ѧ��Ӧ����Ϊ________��
���𰸡��������̺�Ũ����  1.6mol ֤����ˮ�������� ������Ư���ԣ���ˮ��Ư���� �������� E F A 2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O Ca(ClO)2 Ca(ClO)2+CO2+H2O=CaCO3��+2HClO
1.6mol ֤����ˮ�������� ������Ư���ԣ���ˮ��Ư���� �������� E F A 2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O Ca(ClO)2 Ca(ClO)2+CO2+H2O=CaCO3��+2HClO
��������
��. װ��A���Ʊ������ķ���װ�ã����ɵ�������ˮ�������Ȼ��⣬ͨ��װ��B������ͭ��������ˮ����������ˮ������ͨ��E�и������ɫ����������ɫ֤��������Ư���ԣ�ͨ��װ��D��ʪ����ɫ������ɫ��֤��������ˮ��Ӧ���ɵĴ��������Ư���ԣ�ͨ��װ��E�����Ȼ�̼�������������ʣ���Ȼ��ⱻ����������Һ���գ�
��.��1������������Ca��OH��2��Ӧ��д��ѧ����ʽ��
��2��Ư�۵���Ч�ɷ�ΪCa��ClO��2��
��3������Ư���е���Ч�ɷ���CO2���ã������������
��1��ʵ������Ũ����Ͷ������̹�����ȡ���������ӷ�Ӧ����ʽΪ![]() �����ݷ���ʽ��֪ת��0.8mol���ӣ����ĵ�HClΪ1.6mol��
�����ݷ���ʽ��֪ת��0.8mol���ӣ����ĵ�HClΪ1.6mol��
�ʴ�Ϊ���������̺�Ũ���  ��1.6mol��
��1.6mol��
��2������ˮ����ͭ����������ˮ�������ʴ�Ϊ��֤����ˮ����������
��C��D�����������Ƿ���ˮ������ͬ˵���˸��������û��Ư���ԣ�
�ʴ�Ϊ��������Ư���ԣ���ˮ��Ư���ԣ�
��β������������Ҫ���������Ȼ�̼���������������ʴ�Ϊ������������
��3���������Ȼ���ͨ�뵽�������������������Ϊ��ȷ��ʵ����۵Ŀɿ��ԣ�Ӧ��װ��E��F֮������һ��ʢ��ʪ��ĵ��۵⻯����ֽ����ʪ�����ɫ���������ʪ��ĵ��۵⻯����ֽ����������ʪ�����ɫ��������ɫ������������ȫ���գ�
�ʴ�Ϊ��E��F��AC��
��. 1����HClO����Ư�����ã����䲻�ȶ������ñ����ʹ�ã���ҵ�ϳ������������������Ʒ�Ӧ����ȡƯ�ۣ�������Ư��������Cl2��Ca��OH��2��Ӧ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+H2O
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+H2O��
��2�����������Ư�۵���Ч�ɷ֣����Ļ�ѧʽΪCa��ClO��2
�ʴ�Ϊ��Ca��ClO��2��
��3����̼������Աȴ����������ǿ������̼�������Ca��ClO��2��Ӧ��Ca��ClO��2+CO2+H2O=CaCO3+2HClO
�ʴ�Ϊ��Ca��ClO��2+CO2+H2O=CaCO3+2HClO��

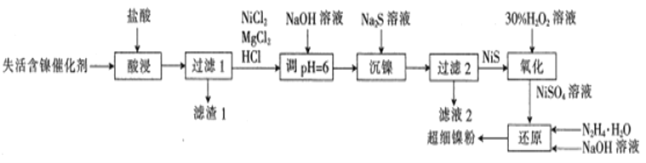
����Ŀ���������ڵ�غ͵�Ƶȹ�ҵ�Ͼ��й㷺����;������Ҳ���к�ǿ�Ķ��ԣ��������л��մ��������Ի�����ɺܴ��Ӱ�죬�������Ե�Ʒ���Ϊԭ�ϻ��NiSO46H2O�Ĺ��̣���֪�������г����������⣬��Ҫ���У�Cu��Zn��Fe��Mg��Ԫ�صĻ����
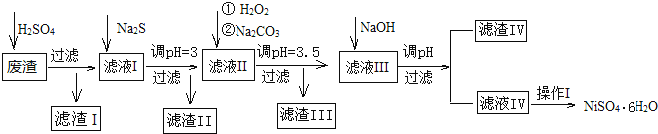
����������������������������ʽ��ȫ����ʱ��Һ��pH������
������ | Fe��OH��3 | Fe��OH��2 | CuS | ZnS | FeS | NiS | Al��OH��3 | Mg��OH��2 | Ni��OH��2 |
pH | 3.2 | 9.7 | ��-0.42 | ��2.5 | ��7 | ��7.5 | ��5 | ��8 | ��8.5 |
��1���������м�H2SO4�����������Ч�ʵķ�����__������д��2�㣩��
��2����Na2Sͬʱ����Һ��pHΪ3��Ŀ���dz�ȥͭ��п�����ʣ�������Һ���м���H2O2�ķ�Ӧ�����ӷ���ʽΪ___��
��3��������������¹��̣�__��__�����ˡ�ϴ�ӡ������ϴ�ӹ��̲�����ˮϴ�ӣ�Ӧ����__ϴ�ӣ�Ŀ����___�������е��¸�����¸���ܷ��ø��¸���___��������____��
��4����Һ���м���NaOH��Һ��Ŀ���ǵ�����Һ��pHΪ8�Գ�ȥAl3+�Լ�������Mg2+��������Mg2+��Al3+����Һ�еμ�NaOH��Һ�������µ����ֳ�����������Һ��pH=8ʱ��c��Mg2+����c��Al3+��=__��{��֪��25��ʱ��Ksp[Mg��OH��2]=5.0��10-14��Ksp[Al��OH��3]=2.0��10-33}��