��Ŀ����
����������Ҫ�ɷ�FeTiO3������������Ϊ��Ҫԭ��ұ�������ѣ������Ĺ�������ͼ���£�������������Ũ���ᷢ����Ӧ�Ļ�ѧ����ʽΪ��
FeTiO3��2H2SO4��TiOSO4��FeSO4��2H2O
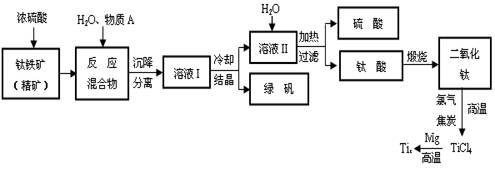
�ش��������⣺
�� �������Ũ���ᷴӦ���� ��ѡ�������ԭ��Ӧ����������ԭ��Ӧ������
���������������м�������A��Ŀ���Ƿ�ֹFe2��������������A�� �������Ʊ�TiO2�Ĺ����У����õ��ĸ�����Ϳɻ������õ����ʷֱ��� ��
�Ƿ�ӦTiCl4��2Mg��2MgCl2��Ti��Ar�����н��е������� ��
���ɶ���������ȡ���Ȼ������漰�ķ�Ӧ�У�
TiO2 (s)+ 2Cl2 (g) +2C(s) ��TiCl4(g) + 2CO(g) ��H1 = -72 kJ��mol-1
TiO2(s) + 2Cl2 (g) ��TiCl4(g) + O2 (g) ��H2 =+38.8kJ��mol��1
C(s)��CO2(g)��2CO(g)??��H3 =+282.8kJ��mol��1
�ٷ�ӦC(s)��CO2(g)��2CO(g)�ڸ������ܹ��Է����е�ԭ���� ��
�ڷ�ӦC(s)��O2(g)��CO2 (g)�Ħ�H�� ��
�ŷ�������ԭ��Ӧ ��Fe �̷������� �Ƿ�ֹ������Mg��Ti��������е���������CO2��N2������ �Ȣ٦�S >0���������ӣ� �ڣ�393.6 kJ��mol ��ÿ��2�֣���12�֣�

 ����ʾ������V������5�ۣ�Ti�ԣ�4�ۣ�Fe�ԣ��ۣ���x��ֵ��_______(�ú�a��b��c�Ĵ���ʽ��ʾ)��
����ʾ������V������5�ۣ�Ti�ԣ�4�ۣ�Fe�ԣ��ۣ���x��ֵ��_______(�ú�a��b��c�Ĵ���ʽ��ʾ)�� ��
�� �����ʣ���д��
�����ʣ���д�� ��ijѧ����ȤС�����һ��ʵ��װ������������Ӧ���Ƶ�
��ijѧ����ȤС�����һ��ʵ��װ������������Ӧ���Ƶ� ��װ����β������������ͼ����ʾ��ƿ��Ӧ����_____________��Һ���ڵ��ܿ�B��Ӧ______________��
��װ����β������������ͼ����ʾ��ƿ��Ӧ����_____________��Һ���ڵ��ܿ�B��Ӧ______________��





 ����ʾ������V������5�ۣ�Ti�ԣ�4�ۣ�Fe�ԣ��ۣ���x��ֵ��_______(�ú�a��b��c�Ĵ���ʽ��ʾ)��
����ʾ������V������5�ۣ�Ti�ԣ�4�ۣ�Fe�ԣ��ۣ���x��ֵ��_______(�ú�a��b��c�Ĵ���ʽ��ʾ)�� ��
�� �����ʣ���д��
�����ʣ���д�� ��ijѧ����ȤС�����һ��ʵ��װ������������Ӧ���Ƶ�
��ijѧ����ȤС�����һ��ʵ��װ������������Ӧ���Ƶ� ��װ����β������������ͼ����ʾ��ƿ��Ӧ����_____________��Һ���ڵ��ܿ�B��Ӧ______________��
��װ����β������������ͼ����ʾ��ƿ��Ӧ����_____________��Һ���ڵ��ܿ�B��Ӧ______________��




