题目内容
实验是研究化学的基础,下列图中所示的实验方法、装置或操作中正确的是.
A、 制取Fe(OH)2 |
B、 测定中和热 |
C、 测定反应速率 |
D、 分离乙醇和乙酸的混合液 |
考点:化学实验方案的评价,物质的分离、提纯的基本方法选择与应用,中和热的测定,测定某些化学反应的速率,制取氢氧化铁、氢氧化亚铁
专题:实验评价题
分析:A.氢氧化亚铁不稳定,易被空气氧化生成氢氧化铁;
B.测定中和热需要使用大小烧杯、环形玻璃搅拌棒、温度计、量筒;
C.长颈漏斗应插入液面以下;
D.分液漏斗分离能分层的物质.
B.测定中和热需要使用大小烧杯、环形玻璃搅拌棒、温度计、量筒;
C.长颈漏斗应插入液面以下;
D.分液漏斗分离能分层的物质.
解答:
解:A.氢氧化亚铁不稳定,易被空气氧化生成氢氧化铁,苯的密度小于水,所以可以用苯隔绝空气的干扰,故A正确;
B.缺少环形玻璃搅拌棒,故B错误;
C.长颈漏斗应插入液面以下,否则会使气体溢出,故C错误;
D.乙醇和乙酸互溶,不能用分液法分离,故D错误.
故选A.
B.缺少环形玻璃搅拌棒,故B错误;
C.长颈漏斗应插入液面以下,否则会使气体溢出,故C错误;
D.乙醇和乙酸互溶,不能用分液法分离,故D错误.
故选A.
点评:本题考查了实验评价,涉及氢氧化亚铁的制备、仪器的使用以及物质的分离提纯等知识点,明确实验原理是解本题关键,根据物质的性质分析解答,易错点为氢氧化亚铁的制取方法、实验操作,题目难度不大.

练习册系列答案
相关题目
化学实验室中常对溶液或试剂进行酸化,下列酸化处理中正确的是( )
| A、定性检验C2H5Cl中的氯元素时,将C2H5Cl和NaOH溶液混合加热,加稀硫酸酸化,再用硝酸银溶液检验 |
| B、鉴别溶液中SO42-和CO32-时,所加的氯化钡溶液可以用盐酸酸化 |
| C、为提高高锰酸钾溶液的氧化能力,用浓盐酸将高锰酸钾溶液酸化 |
| D、实验室在配置Fe2(SO4)3溶液时,通常滴加几滴稀硫酸酸化 |
俗话说“雷雨发庄稼”.在雷雨天,空气中有O3(由O2生成)和NO产生,下列说法正确的是( )
| A、NO在空气中不能稳定存在,会继续反应 |
| B、生成O3和NO的反应都是氧化还原反应 |
| C、O3和O2两种气体都是氧元素形成的单质,化学性质相同 |
| D、NO的产生是形成酸雨的主要原因 |
VmL Al2(SO4)3溶液中,含有Al3+a g,取
mL溶液稀释到3V mL,则稀释后溶液中
的物质的量浓度是( )
| V |
| 2 |
| SO | 2- 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组物质互为同分异构体的是( )
| A、H2O和H2O2 |
| B、己烷与环己烷 |
C、 与CH3CH2CH2CH3 与CH3CH2CH2CH3 |
| D、氰酸铵NH4CNO与尿素CO(NH2)2 |
下列气体实验中,正确的是( )
A、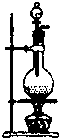 铜和稀硝酸制一氧化氮气体 |
B、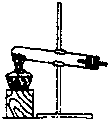 加热Cu(NO3)2(s)获取NO2(g) |
C、 浓硫酸滴入浓盐酸中制HCl |
D、 硫化氢气体的干燥与收集 |
燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量乙烯所产生的CO2的量,该混合气体是( )
| A、乙烯、丙烷 |
| B、苯、乙烯 |
| C、甲烷、丙烷 |
| D、乙烷、环丙烷(C3H6) |
下列有关实验的叙述正确的是( )
| A、用HF溶液可以除去硅晶体中含有的少量二氧化硅晶体 |
| B、向两份Fe3O4固体中分别加入HCl溶液与HI溶液,二者反应现象一样 |
| C、向某溶液中滴加NaOH溶液后又加入酚酞,溶液呈红色,说明原溶液中含有NH4+ |
| D、向某溶液中加入足量的稀HNO3溶液,所得气体能使澄清石灰水变浑浊,证明该溶液中存在CO32-或HCO3- |
下列叙述不正确的是( )
A、 放电闪电时会发生反应: N2+O2═2NO |
B、 利用丁达尔效应证明烧杯中的分散系是胶体 |
C、 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 |
D、 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |