题目内容
20.在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)?2Z(g)此反应达到平衡的标志是( )| A. | 容器内压强不随时间变化 | |
| B. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| C. | 容器内各物质的浓度不随时间变化 | |
| D. | 单位时间消耗0.1molX同时生成0.2molZ |
分析 可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析解答.
解答 解:A、反应前后气体物质的量不同,所以压强不变说明各组分浓度不变,反应到达平衡状态,故A正确;
B、XYZ的浓度大小决定于开始加入的多少,与平衡状态无关,故B错误;
C、容器内X、Y、Z的浓度不随时间变化,说明反应达到平衡,故C正确;
D、单位时间消耗0.1molX同时生成0.2molZ,说明反应v正(X)=2v正(Y),不能说明达平衡,故D错误;
故选AC.
点评 在利用速率判断平衡时,必须有v正和v逆,同种物质相等,不同物质等于系数之比,题目难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
10.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )


| A. | 石墨和金刚石的转化是物理变化 | |
| B. | 金刚石的稳定性强于石墨 | |
| C. | 石墨和金刚石是同分异构体 | |
| D. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 |
8.把一块生锈的铁片投入盛有稀硫酸溶液的烧杯里,待铁片完全溶解后,往烧杯里滴加氢氧化钠溶液至过量,然后过滤,并充分灼烧不溶物,则最终留下的固体是( )
| A. | Na2O | B. | Fe2O3和Fe | C. | Fe2O3 | D. | Fe2O3和NaOH |
15.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,22g CO2含有原子数1.5NA | |
| C. | 32g 氧气和臭氧的混合气体中含有氧原子的个数为2NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
5.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 2.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.04NA | |
| C. | 7.8g Na2S和Na2O2的固体混合物中含有的阴离子数等于0.1NA | |
| D. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
10.下列变化中,涉及不到化学变化的是( )
| A. | 石油的分馏 | B. | 氯气溶于水 | C. | 食物腐败 | D. | 煤的干馏 |
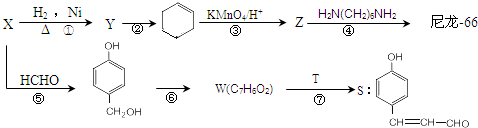
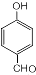 ,T的分子式为C2H4O.
,T的分子式为C2H4O.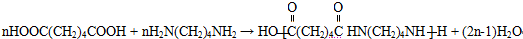 .
.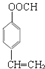 .
.