题目内容
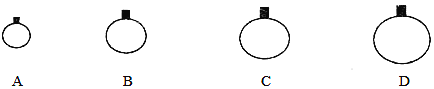
【题目】(1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_________(填选项序号)。
(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为_______。
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7molL﹣1,c(Zn2+)=0.1molL﹣1,c(Cl﹣)=0.3molL﹣1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为_________。
(4)0.3mol的甲烷与_________g氨气中所含氢原子数相等。
(5)在同温同压下,2g二氧化碳的体积为120ml,而2gA气体的体积为165ml,则气体A的摩尔质量_________________;
(6)标准状况下,11.2L二氧化碳和一氧化碳混合气体的质量为18g,则其中二氧化碳的质量为_________,一氧化碳的体积为_________。
(7)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100molL﹣1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl﹣,则S2O32﹣将转化成____________。
A.S2﹣ B.S C.SO32﹣ D.SO42﹣
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移0.6mole﹣,则被氧化的HCl的物质的量为_____________。
【答案】A 2.8g 0.03mol 6.8 32g/mol 11g 5.6L D 0.6mol
【解析】
(1)等质量的CH4、CO2、O2、SO2四种气体的物质的量与其摩尔质量成反比,即摩尔质量越大,则物质的量越小,在同温同压下,体积越小,据此进行解答;
(2)在标准状况下,2.24L由N2、N2O组成的混合气体物质的量n=V/Vm,据m=nM来计算质量即可;
(3)根据溶液中各种离子遵循电荷守恒来回答判断;
(4)根据0.3mol的甲烷含有氢原子物质的量计算氨气的物质的量,根据m=nM计算氨气的质量;
(5)结合n=![]() =
=![]() 计算;
计算;
(6)根据n=![]() 进行相关物理量的计算,可设CO为xmol,CO2为ymol,列方程式计算。
进行相关物理量的计算,可设CO为xmol,CO2为ymol,列方程式计算。
(7)①在氧化还原反应中,化合价降低总数=化合价升高总数=转移电子数,根据转移电子相等确定生成物;
②反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移6mole-,则被氧化的HCl的物质的量是6mol,据此回答。
(1)气体的物质的量n=![]() ,在同温同压下,气体摩尔体积相同,气体的体积V=nVm,即V=
,在同温同压下,气体摩尔体积相同,气体的体积V=nVm,即V=![]() Vm可知,摩尔质量越大,体积越小;CH4、CO2、O2、SO2的摩尔质量分别为16g/mol、44g/mol、32g/mol、64g/mol,SO2的摩尔质量最大,故体积最小,故A正确,故答案为A;
Vm可知,摩尔质量越大,体积越小;CH4、CO2、O2、SO2的摩尔质量分别为16g/mol、44g/mol、32g/mol、64g/mol,SO2的摩尔质量最大,故体积最小,故A正确,故答案为A;
(2)在标准状况下,2.24L由N2、N2O组成的混合气体物质的量n=V/Vm=0.1mol,据m=nM=0.1mol×2×14g/mol=2.8g;
(3)溶液中各种离子遵循电荷守恒,2c(SO42- )+c(Cl-)=2c(Zn2+)+c(K+),解得2c(SO42- )=0.1×2+0.7-0.3=0.6mol/L,c(SO42- )=0.3mol/L,则n(SO42- )=0.3mol/L×0.1L=0.03mol,加入氯化钡产生硫酸钡的物质的量为0.03mol;
(4)与0.3molCH4分子中所含氢原子数相等的氨气物质的量=![]() =0.4mol,故氨气的质量=0.4mol×17gmol-1=6.8g;
=0.4mol,故氨气的质量=0.4mol×17gmol-1=6.8g;
(5)n(CO2)=![]() =
=![]() mol,Vm=
mol,Vm=![]() =
= =2.64L/mol,则n(A)=
=2.64L/mol,则n(A)=![]() =0.0625mol,M(A)=
=0.0625mol,M(A)=![]() =32g/mol;
=32g/mol;
(6)气体的物质的量为n=![]() =
=![]() =0.5mol,设CO为xmol,CO2为ymol,则:28x+44y=18、x+y=0.5,解得:x=0.25、y=0.25;故m(CO2)=0.25mol×44g/mol=11g,n(CO)=0.25mol,V(CO)=0.25mol×22.4L/mol=5.6L;
=0.5mol,设CO为xmol,CO2为ymol,则:28x+44y=18、x+y=0.5,解得:x=0.25、y=0.25;故m(CO2)=0.25mol×44g/mol=11g,n(CO)=0.25mol,V(CO)=0.25mol×22.4L/mol=5.6L;
(4)①n(Na2S2O3)=0.1mol/L×0.025L=0.0025mol,氯气的物质的量=0.01mol,二者完全反应时转移电子相等,设硫代硫酸根离子被氧化后硫元素的化合价为x,
0.01mol×2×(1-0)=0.0025mol×2×(x-2),4=x-2,x=+6,所以硫代硫酸根离子转化为硫酸根离子,故答案为:D;
②反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移6mole-,则被氧化的HCl的物质的量是6mol,若反应中转移0.6mole-,则被氧化的HCl的物质的量是0.6mol。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案【题目】甲醇是重要的化学工业基础原料和清洁液体燃料。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度/℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=________(用K1、K2表示)。
(2)反应③的ΔH_________0(填“>”或“<”)。
(3)500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时υ正_____υ逆(填“>”、“=”或“<”)。
(4)500℃时2L密闭容器中投入a mol H2、b mol CO发生反应①;测得平衡时H2(g)、CO(g)的浓度(mol·L-1)分别为0.2、0.1则:
①平衡时H2的转化率为________(保留一位有效数字)。
②若向平衡后的容器中再投入a mol H2、b mol CO,达平衡后,CH3OH的体积分数与原平衡相比______________(填“增大”、“减小”或“不变”)