题目内容
3.下列有关化学用语的表示方法中错误的是( )| A. | CO2分子的结构式:O=C=O | |
| B. | 次氯酸的电子式: | |
| C. | R2+离子核外有a个电子,b个中子,R原子符合为:${\;}_{a+2}^{a+b+2}$R | |
| D. | S2-的结构示意图: |
分析 A.二氧化碳是直线形结构,每个氧原子和碳原子形成碳氧双键;
B.次氯酸的中心原子是氧原子;
C.质子数+中子数=质量数,阳离子质子数=核外电子数+所带电荷数;
D.硫离子含有16个质子,核外有18个电子.
解答 解:A.二氧化碳是直线形结构,每个氧原子和碳原子形成碳氧双键,其结构式为:O=C=O,故A正确;
B.次氯酸的中心原子是氧原子,次氯酸的电子式为: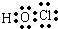 ,故B错误;
,故B错误;
C.R2+离子核外有a个电子,b个中子,质子数为:a+2,质量数为:2+a+b,R原子符合为:${\;}_{a+2}^{a+b+2}$R,故C正确;
D.硫离子含有16个质子,核外有18个电子,结构示意图: ,故D正确;
,故D正确;
故选:B.
点评 本题考查了化学用语,涉及电子式的书写、结构式的书写、原子结构示意图、原子符合的表示,侧重考查学生对基础知识的掌握熟练程度,题目难度不大.

练习册系列答案
相关题目
13.理论上不能用设计成原电池的反应是( )
| A. | CaO+H2O═Ca(OH)2△H<0 | B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H<0 | ||
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4 Fe(OH)3(s)△H<0 | D. | 2H2(g)+O2(g)═2H2O(l)△H<0 |
14.在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)=S(g)+H2O(g)△H3
④S(g)=$\frac{1}{2}$S2(g)△H4
则△H4的正确表达式为( )
①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)=S(g)+H2O(g)△H3
④S(g)=$\frac{1}{2}$S2(g)△H4
则△H4的正确表达式为( )
| A. | △H4=$\frac{1}{3}$(△H1+△H2-3△H3) | B. | △H4=$\frac{1}{3}$(3△H3-△H1-△H2) | ||
| C. | △H4=$\frac{3}{4}$(△H1+△H2-3△H3) | D. | △H4=$\frac{3}{4}$(△H1-△H2-3△H3) |
11.下列物质中,由原子直接构成的是( )
| A. | 金刚石 | B. | 氯化钠 | C. | 氧气 | D. | 水 |
18.下列实验方案中,合理的是( )
| A. | 分离木炭粉和CuO:在空气中充分灼烧 | |
| B. | 验证质量守恒定律:比较镁条燃烧前后固体质量 | |
| C. | 制备Fe(OH)3:向FeCl3溶液中加入NaOH溶液,过滤、洗涤、干燥 | |
| D. | 除去CO2中的HCl和水蒸气:依次通过过量的NaOH溶液、浓硫酸 |
8.1mol D2O和1mol H2O中不相同的是( )
| A. | 含氧原子的数目 | B. | 含有电子的数目 | C. | 含有质子的数目 | D. | 含有中子的数目 |
15.以下化学用语正确的是( )
| A. | 羟基的电子式: | B. | 乙醇的结构式CH3CH2OH | ||
| C. | 乙烷的结构简式CH3CH3 | D. | 聚丙烯的结构简式: |
12.下列各物质无论以何种比例混合,其氯元素的质量分数不变的是( )
| A. | HClO4、KClO3 | B. | KClO、KCl | C. | NaClO、KCl | D. | NaCl、KCl |
13.从原子序数11依次增加到17,下列所叙递变关系错误的是( )
| A. | 金属性逐渐增强 | B. | 原子半径逐渐增大 | ||
| C. | 最高正价数值逐渐增大 | D. | 从硅到氯负价从-4-1 |