题目内容
【题目】物质A-K有如图所示转化关系,其中气体D、E为单质,试回答下列问题:
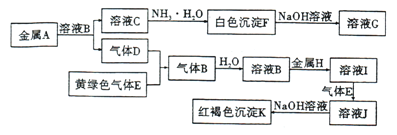
(1)写出下列物质的化学式:气体D是________,H是________.
(2)写出反应“I![]() J”的离子方程式:__________
J”的离子方程式:__________
(3)写出反应“F![]() G" 的离子方程式:____________
G" 的离子方程式:____________
(4)在溶液I中滴人NaOH溶液,可观察到的现象是_______其反应的原理是_________(写化学方程式)。
(5)检验溶液J中的金属阳离子,用_______试剂(填化学式),其现象是__________。
【答案】 H2 Fe 2Fe2++Cl2=2Fe3++2Cl- Al(OH)3+OH-=AlO2-+2H2O 先生成白色沉淀然后变为灰绿色,最后变为红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3 KSCN 溶液变为血红色
【解析】K为红褐色沉淀,则应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2,E应为氧化性气体Cl2,B应为HCl,H为Fe,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3,
(1)由以上分析可知D应为H2,H为Fe;(2)反应“I→J”是FeCl2和Cl2发生反应生成氯化亚铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-;(3)“F→G”的离子方程式:Al(OH)3+OH-=AlO2-+2H2O;(4)在溶液I中滴入NaOH溶液,可观察到的现象是:先出现白色沉淀,随即变成灰绿色,最后变成红褐色。其反应的原理是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(6)检验溶液J中的金属阳离子即Fe3+,可取溶液加入KSCN溶液,溶液变为血红色,证明含有Fe3+。

【题目】将物质X逐渐加入(或通入)Y溶液中,其生成沉淀的量与加入X的物质的量的关系如下图所示,符合图示情况的是( )
| A | B | C | D |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A. A B. B C. C D. D



