题目内容
工业上制备BaCl2的工艺流程图如下:
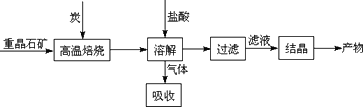
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验.查表得BaSO4(s)+4C(s)![]() 4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1①
4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1①
BaSO4(s)+2C(s)![]() 2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠.
Na2S水解的离子方程式为________.
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,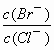 =________.
=________.
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的是________.
答案:
解析:
解析:
|
(1)S2-+H2O (2)2.7×10-3(5分) (3)使BaSO4得到充分的还原(或提高BaS的产量) ①②为吸热反应,炭和氧气反应放热维持反应所需高温(5分) |

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
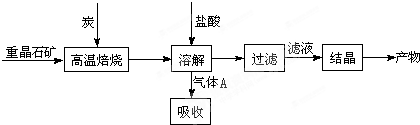
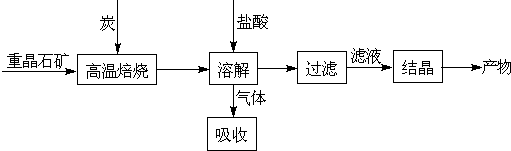
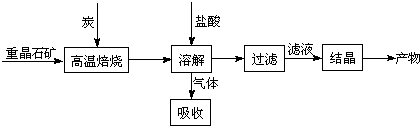
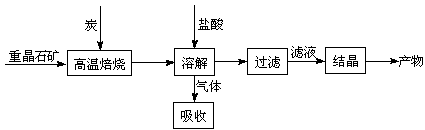
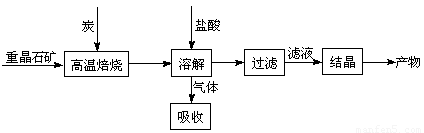
 4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ①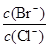 =
。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
=
。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]