题目内容
检验某无色溶液中是否含有SO42-,下列操作中最合理的是( )
| A、加入硝酸酸化了的硝酸钡溶液 |
| B、先加硝酸酸化,再加硝酸钡溶液 |
| C、先加盐酸酸化,再加氯化钡溶液 |
| D、加入盐酸酸化了的氯化钡溶液 |
考点:硫酸根离子的检验
专题:物质检验鉴别题
分析:检验无色溶液中是否含有SO42-时要注意排除 SO32-、CO32- 等离子的影响.
解答:
解:A、加入稀硝酸酸化的硝酸钡溶液,亚硫酸根离子会被氧化为硫酸根离子,不能排除亚硫酸根离子的干扰,故A错误;
B、先加稀硝酸,硝酸可以将亚硫酸根离子氧化成硫酸根离子,再加入硝酸钡溶液,产生硫酸钡沉淀,故B错误;
C、先加稀盐酸,可以排除银离子与碳酸根离子,再加入氯化钡溶液,产生的沉淀只能是硫酸钡,故C正确;
D、加入氯化钡和盐酸的混合溶液,不能排除银离子的干扰,故D错误.
故选:C.
B、先加稀硝酸,硝酸可以将亚硫酸根离子氧化成硫酸根离子,再加入硝酸钡溶液,产生硫酸钡沉淀,故B错误;
C、先加稀盐酸,可以排除银离子与碳酸根离子,再加入氯化钡溶液,产生的沉淀只能是硫酸钡,故C正确;
D、加入氯化钡和盐酸的混合溶液,不能排除银离子的干扰,故D错误.
故选:C.
点评:在实验设计中若不能考虑到物质和微粒的干扰,则无法对结论进行准确的定性.所以实验中要注意考虑彼此微粒和物质之间的干扰.平时练习中要勤于总结,注意存在干扰的物质和微粒的处理.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
用铁片与稀硫酸反应制备氢气,下列措施不能使氢气生成速率加快的是( )
| A、铁片改为铁粉 |
| B、稀硫酸改为98% 浓硫酸 |
| C、对该反应体系加热 |
| D、铁片改为锌片 |
对于可逆反应2SO2+O2?2SO3达到平衡的标志是( )
| A、SO2、O2、SO3的物质的量浓度不再变化 |
| B、O2和SO3的化学反应速率相等 |
| C、SO2、O2、SO3的分子数之比为2:1:2 |
| D、单位时间生成2n mol SO2,同时生成n mol O2 |
可逆反应A(g)+B?C(g)+D中,A、C都是无色气体,当达到平衡时,下列叙述不正确的是( )
| A、若增大A的浓度,平衡体系颜色加深,说明D是有颜色的气体 |
| B、增大压强,平衡不移动,说明B、D必是气体 |
| C、若B是气体,增大A的浓度会使B的转化率增大 |
| D、升温,C的质量分数减小,说明逆反应是放热反应 |
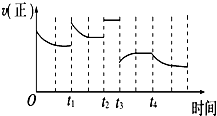 合成氨反应:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如图,下列说法正确的是( )
合成氨反应:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1,在反应过程中,正反应速率的变化如图,下列说法正确的是( )| A、t1时升高了温度 |
| B、t2时使用了催化剂 |
| C、t3时降低了温度 |
| D、t4时减小了压强 |
 乙醛在空气中易被氧化,沸点为20.8℃.40%的乙醛溶液久置会分层,其上层为无色油状液体.经测定无色油状液体为乙醛的自身加成物(C2H4O)n,其沸点比水的沸点高,分子中无醛基.现根据反应原理:(C2H4O)n
乙醛在空气中易被氧化,沸点为20.8℃.40%的乙醛溶液久置会分层,其上层为无色油状液体.经测定无色油状液体为乙醛的自身加成物(C2H4O)n,其沸点比水的沸点高,分子中无醛基.现根据反应原理:(C2H4O)n