题目内容
11.下列关于电解质说法正确的是( )| A. | 能导电的物质叫电解质 | |
| B. | NaCl晶体不导电,所以NaCl不是电解质 | |
| C. | 熔融的KOH导电,所以KOH是电解质 | |
| D. | 电解质在通电时发生电离 |
分析 A.金属单质能导电,单质不属于电解质;
B.晶体中不存在自由移动的离子;
C.在水溶液中或熔化状态下能导电的化合物为电解质;
D.电解质溶于水或熔化下能电离,不需要另外通电.
解答 解:A.金属单质能导电,但金属单质不是电解质,故A错误;
B.NaCl晶体中有离子,但不存在自由移动的离子,则不导电,但NaCl为电解质,故B错误;
C.在水溶液中或熔化状态下能导电的化合物为电解质,则熔融的KOH导电,所以KOH是电解质,故C正确;
D.电解质溶于水或熔化下能电离,不需要通电,故D错误;
故选C.
点评 本题考查电解质的导电及电解质的判断,题目难度不大,明确电解质为化合物及电解质电离的条件即可解答,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
1.下列有关化学用语的表示正确的是( )
| A. | NH4Br的电子式:[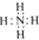 ]+Br- ]+Br- | |
| B. | S2-的结构示意图: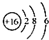 | |
| C. | 原子核内有18个中子的氯分子:${\;}_{17}^{35}$Cl2 | |
| D. | 水分子的形成过程用电子式表示为:H2+ → → |
2.关于下列各装置图的叙述中,不正确的是( )
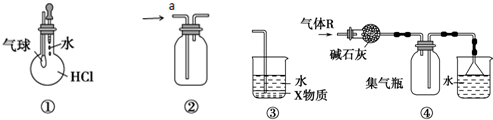

| A. | 装置①可验证HCl气体在水中的溶解性 | |
| B. | 装置②a口进气可用于收集CO2、Cl2或NO等 | |
| C. | 装置③中X为四氯化碳,可用于吸收氨气或氯化氢 | |
| D. | 装置④可用于干燥、收集氨气,并吸收多余的氨气 |
16.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
3.根据表中信息,判断以下叙述正确的是部分短周期元素的原子半径及主要化合价( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | 单质与稀盐酸反应的剧烈程度为L<Q | |
| C. | R最高价氧化物对应水化物是强酸 | |
| D. | L2+与R2-的核外电子数相等 |
20.化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A. | 纤维素在人体内不能被消化吸收,可帮助消化 | |
| B. | 可以用Si3N4、Al2O3制作高温结构陶瓷制品 | |
| C. | 在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 | |
| D. | 禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
1.下列各组离子在溶液中可以大量共存的是( )
| A. | Mg2+、Fe3+、Cl-、OH- | B. | Ba2+、HCO3-、Cl-、Na+ | ||
| C. | Fe2+、SO42-、H+、NO3- | D. | K+、NH4+、SO42-、OH- |