题目内容
13.10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如表变化:| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
分析 (1)水解是吸热过程,升温HCO3-的水解程度增大,故碱性增强,碳酸氢根离子水解生成碳酸和氢氧根离子;
(2)碳酸钠是强碱弱酸盐能水解,且碳酸钠的水解程度大于碳酸氢钠的水解程度;
(3)依据冷却到室温溶液PH中的分析反应过程中生成了新的物质;碳酸钠水解程度大于碳酸氢钠,溶液减小增强.
解答 解:(1)碳酸氢钠是强碱弱酸酸式盐,能水解导致溶液呈碱性,升高温度,HCO3-的水解程度增大,故碱性增强,水解方程式为:HCO3-+H2O?H2CO3+OH-;
故答案为:HCO3-+H2O?H2CO3+OH-;
(2)碳酸钠是强碱弱酸盐能水解,碳酸是二元弱酸,第一步电离程度远远大于第二步电离,所以碳酸根离子的第一步水解程度远远大于第二步水解程度,导致碳酸钠的水解程度大于碳酸氢钠的水解程度,
故答案为:大于;
(3)将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1,溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成;所以乙正确;
故答案为:乙;溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成.
点评 本题碳酸氢钠考查了碳酸氢钠的性质,实验探究物质性质的设计方案,反应产物的判断,盐类水解的分析应用,题目难度中等.

练习册系列答案
相关题目
3.液氨和水类似,也能电离:NH3+NH3?NH4++NH2-,25℃时,其离子积K=1.0×10-30 mol2•L-2.现将2.3g金属钠投入1.0L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中不存在的关系式是(设温度保持不变,溶液体积为1L)( )
| A. | c(Na+)=c(NH2-) | B. | c(NH4+)=1×10-29 mol•L-1 | ||
| C. | c(NH2-)>c(NH4+) | D. | c(NH4+).c(NH2-)=1.0×10-30 mol2•L-2 |
2.已知某无色溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是( )
| A. | CO32-、Cl- | B. | Na+、Cu2+ | C. | Mg2+、C1- | D. | C1-、Ba2+ |
10.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 当转移8mol电子时,还原产物比氧化产物多1mol |
 (3)装置B中试剂的作用是检验SO2是否除尽.
(3)装置B中试剂的作用是检验SO2是否除尽.

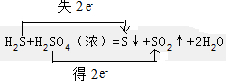 .
.