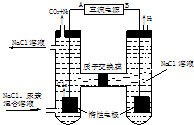
ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩSΓΔNΓΔClΕΦ «÷Ί“ΣΒΡΖ«Ϋπ τ‘ΣΥΊΘ§œ¬Ν–ΥΒΖ®’ΐ»Ζ «Θ®ΓΓΓΓΘ©
A.98%ΒΡ≈®ΝρΥα”ΟΒ»ΧεΜΐΒΡΥ°œΓ ΆΚσΘ§ΝρΥαΒΡ÷ ΝΩΖ÷ ΐΈΣ49%
B.SO32©¹ΓΔClO©¹ΓΔNO3©¹»ΐ÷÷άκΉ”‘Ύ»ή“Κ÷–“ρΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΕχ≤ΜΡή¥σΝΩΙ≤¥φ
C.≈®ΝρΥαΓΔœθΥαΨΏ”–«Ω―θΜ·–‘Θ§≈®œθΥαΚΆ≈®―ΈΥα“ΉΖ÷ΫβΨΏ”–≤ΜΈ»Ε®–‘
D.±ξΩωœ¬Θ§22.4L¬»Τχ”κΉψΝΩ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΘ§ΉΣ“ΤΒΡΒγΉ” ΐΈΣ2NAΗωΘ®NAΈΣΑΔΖϋΦ”Β¬¬ό≥Θ ΐΘ©
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩAΘ°ΜλΚœΚσ»ή“Κ÷–»ή÷ ΝρΥαΒΡ÷ ΝΩΒ»”Ύ‘≠≈®ΝρΥα÷–»ή÷ ΝρΥαΒΡ÷ ΝΩΘ§Υ°ΒΡΟήΕ»–Γ”Ύ≈®ΝρΥαΒΡΟήΕ»Θ§Β»ΧεΜΐΜλΚœΚσ»ή“ΚΒΡ÷ ΝΩ–Γ”Ύ≈®ΝρΥα÷ ΝΩΒΡ2±ΕΘ§Ι ΜλΚœΚσΝρΥαΒΡ÷ ΝΩΖ÷ ΐ¥σ”Ύ49%Θ§Ι A¥μΈσΘΜ
BΘ°ClO©¹ΨΏ”–«Ω―θΜ·–‘Θ§Ω…“‘―θΜ·SO32©¹ Θ§ ΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΕχ≤ΜΡή¥σΝΩΙ≤¥φΘ§Ι B’ΐ»ΖΘΜ
CΘ°≈®ΝρΥαΓΔœθΥαΨΏ”–«Ω―θΜ·–‘Θ§≈®œθΥα“ΉΖ÷ΫβΨΏ”–≤ΜΈ»Ε®–‘Θ§ΒΪ≈®―ΈΥα“ΉΜ”ΖΔΘ§HCl≤Μ“ΉΖ÷ΫβΘ§Έ»Ε®–‘«ΩΘ§Ι C¥μΈσΘΜ
DΘ°±ξΩωœ¬Θ§22.4L¬»ΤχΒΡΈο÷ ΒΡΝΩΈΣ1molΘ§ΖΔ…ζΖ¥”ΠCl2+2NaOH=NaCl+NaClO+H2OΘ§Ζ¥”Π÷–¬»ΤχΤπ―θΜ·ΦΝΓΔΜΙ‘≠ΦΝΉς”ΟΘ§Ης’Φ“ΜΑκΘ§Ι ΒγΉ”ΉΣ“Τ ΐΡΩΈΣ1molΓΝ![]() ΓΝ2ΓΝNAmol©¹1=NA Θ§ Ι D¥μΈσΘΜ
ΓΝ2ΓΝNAmol©¹1=NA Θ§ Ι D¥μΈσΘΜ
Ι ―ΓBΘ°

ΓΨΧβΡΩΓΩ‘Ύ“ΜΕ®Έ¬Ε»œ¬Θ§ΫΪΤχΧεXΚΆΤχΧεYΗς0.16mol≥δ»κ10LΚψ»ίΟή±’»ίΤς÷–Θ§ΖΔ…ζΖ¥”ΠXΘ®gΘ©+YΘ®gΘ©2ZΘ®gΘ©ΘΜΓςHΘΦ0Θ§“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ°Ζ¥”ΠΙΐ≥Χ÷–≤βΕ®ΒΡ ΐΨί»γœ¬±μΘΚ
t/min | 2 | 4 | 7 | 9 |
nΘ®YΘ©/mol | 0.12 | 0.11 | 0.10 | 0.10 |
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.0ΓΪ2 minΒΡΤΫΨυΥΌ¬ vΘ®ZΘ©=2.0ΓΝ10©¹3 molL©¹1min©¹1
B.ΤδΥϊΧθΦΰ≤Μ±δΘ§ΫΒΒΆΈ¬Ε»Θ§Ζ¥”Π¥οΒΫ–¬ΤΫΚβ«Α vΘ®’ΐΘ©ΘΦvΘ®ΡφΘ©
C.ΗΟΈ¬Ε»œ¬¥ΥΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK=144
D.ΤδΥϊΧθΦΰ≤Μ±δΘ§‘Ό≥δ»κ0.2 mol ZΘ§ΤΫΚβ ±XΒΡΧεΜΐΖ÷ ΐ≤Μ±δ
ΓΨΧβΡΩΓΩΈ¬Ε»ΈΣT ±Θ§œρ2.0LΚψ»ίΟή±’»ίΤς÷–≥δ»κ1.0mol PCl5 Θ§ Ζ¥”ΠPCl5Θ®gΘ©PCl3Θ®gΘ©+Cl2Θ®gΘ©Ψ≠“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΘ°Ζ¥”ΠΙΐ≥Χ÷–≤βΕ®ΒΡ≤ΩΖ÷ ΐΨίΦϊœ¬±μΘΚ
t/s | 0 | 50 | 150 | 250 | 350 |
nΘ®PCl3Θ©/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.Ζ¥”Π‘Ύ«Α50sΒΡΤΫΨυΥΌ¬ ΈΣvΘ®PCl3Θ©=0.0032molL©¹1s©¹1
B.±Θ≥÷ΤδΥϊΧθΦΰ≤Μ±δΘ§…ΐΗΏΈ¬Ε»Θ§ΤΫΚβ ±Θ§cΘ®PCl3Θ©=0.11molL©¹1 Θ§ ‘ρΖ¥”ΠΒΡΓςHΘΦ0
C.œύΆ§Έ¬Ε»œ¬Θ§Τπ Φ ±œρ»ίΤς÷–≥δ»κ1.0mol PCl5ΓΔ0.20mol PCl3ΚΆ0.20mol Cl2 Θ§ ¥οΒΫΤΫΚβ«ΑvΘ®’ΐΘ©ΘΨvΘ®ΡφΘ©
D.œύΆ§Έ¬Ε»œ¬Θ§Τπ Φ ±œρ»ίΤς÷–≥δ»κ2.0mol PCl3ΓΔ2.0mol Cl2 Θ§ ¥οΒΫΤΫΚβ ±Θ§PCl3ΒΡΉΣΜ·¬ –Γ”Ύ80%