题目内容
在一定体积密闭容器中,进行如下反应:
CO2(g) + H2(g)  CO(g) + H2O(g),
CO(g) + H2O(g),
其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2) 该反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否达到化学平衡状态的依据
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4)在830℃时,若起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,反应达到平衡时,CO的转化率为 。
(1)K= 
(2) 吸热
(3)B C
(4)50%
解析试题分析:(1) K的表达式为K=  ;(2)可以知道,温度越高,K越大,所以该反应为吸热反应;(3) 能判断该反应是否达到化学平衡状态的依据为混合气体中CO浓度不变、v(H2)正 = v(H2O)逆,故BC正确,A错误,因为反应一直都是压强不变,不能用来做为达到平衡状态的依据,D也错误,c(CO2) = c(CO)只是某个过程中的条件,不能用来做为达到平衡状态的依据;(4)由表可以知道,在830℃时,K为1,所以
;(2)可以知道,温度越高,K越大,所以该反应为吸热反应;(3) 能判断该反应是否达到化学平衡状态的依据为混合气体中CO浓度不变、v(H2)正 = v(H2O)逆,故BC正确,A错误,因为反应一直都是压强不变,不能用来做为达到平衡状态的依据,D也错误,c(CO2) = c(CO)只是某个过程中的条件,不能用来做为达到平衡状态的依据;(4)由表可以知道,在830℃时,K为1,所以
K=  =1,起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,平衡时,各物质的的浓度为a,则(1-a)(1-a)/(a×a)=1,所以a为0.5mol·L—1,所以CO的转化率为50%。
=1,起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,平衡时,各物质的的浓度为a,则(1-a)(1-a)/(a×a)=1,所以a为0.5mol·L—1,所以CO的转化率为50%。
考点:化学平衡
点评:本题考查了化学平衡的知识,是高考考查的重点,该题比较容易。

 阅读快车系列答案
阅读快车系列答案在一定体积密闭容器中,进行如下反应: CO2(g)+ H2(g) CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1) K的表达式为:
(2) 该反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否达到化学平衡状态的依据
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) =c(CO)
(4) 在830℃时,若起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,反应达到平衡时,CO的转化率为 。
在一定体积密闭容器中,进行如下反应: CO2(g)
+ H2(g) 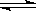 CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1) K的表达式为:
(2) 该反应为 反应(“吸热”或“放热”)
(3) 能判断该反应是否达到化学平衡状态的依据
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4) 在830℃时,若起始浓度c(CO)为1mol·L—1,c(H2O)为1mol·L—1,反应达到平衡时,CO的转化率为 。