题目内容
化合物A由两种常见元素组成,且A中两种元素的质量比为4:1.A有如图所示转化关系,其中B、F均为红色固体,C能使品红溶液褪色(有的反应可能在水溶液中进行,有的反应的生成物未全部给出).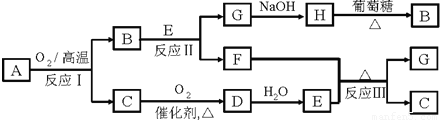
(1)写出下列物质的化学式,A______,B______,H______.
(2)反应I中还原剂与氧化剂的物质的量之比为______,
反应Ⅱ的离子方程式为______.
反应Ⅲ的化学方程式为______ CuSO4+SO2↑+2H2O
【答案】分析:(1)H和葡萄糖反应生成B为红色固体,则H为Cu(OH)2,B为Cu2O,在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,则E为酸,F为Cu,由C→D→E等反应可知,C为SO2,D为SO3,E为H2SO4,则G为CuSO4,A应含有Cu和S两种元素,质量比为4:1,应为Cu2S;
(2)根据物质的性质书写有关反应的离子方程式并判断氧化剂和还原剂之间的关系;
(3)通入氧气的一极为原电池的正极,发生还原反应,负极发生氧化反应;
(4)①根据浓度的变化计算反应速率,根据平衡常数等于生成物浓度幂之积除以反应物浓度幂之积计算;
②计算出该温度时的平衡常数,根据温度对平衡移动的影响判断.
解答:解:(1)H和葡萄糖反应生成B为红色固体,则H为Cu(OH)2,B为Cu2O,在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,则E为酸,F为Cu,由C→D→E等反应可知,C为SO2,D为SO3,E为H2SO4,则G为CuSO4,A应含有Cu和S两种元素,质量比为4:1,应为Cu2S,故答案为:Cu2S;Cu2O;Cu(OH)2;
(2)反应Ⅰ为:2Cu2S+3O2 2Cu2O+2SO2,由方程式可以看出,还原剂与氧化剂的物质的量之比为2:3,Cu2O在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,Cu和浓硫酸在加热条件下反应生成CuSO4和SO2,反应的化学方程式为Cu+2H2SO4(浓)
2Cu2O+2SO2,由方程式可以看出,还原剂与氧化剂的物质的量之比为2:3,Cu2O在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,Cu和浓硫酸在加热条件下反应生成CuSO4和SO2,反应的化学方程式为Cu+2H2SO4(浓)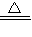 CuSO4+SO2↑+2H2O,
CuSO4+SO2↑+2H2O,
故答案为:2:3;Cu2O+2H+=Cu+Cu2++H2O;Cu+2H2SO4(浓)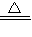 CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3)氧气具有氧化性,应为原电池的正极,发生还原反应,二氧化硫具有还原性,应为原电池的负极,发生氧化反应,电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:正;SO2+2H2O-2e-=SO42-+4H+;
(4)①c(SO2)=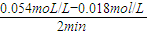 =0.018mol/(L?min),
=0.018mol/(L?min),
2SO2+O2 2SO3
2SO3
起始:0.054mol/L 0.032mol/L
转化:0.048mol/L 0.024mol/L 0.048mol/L
平衡:0.006moL/L 0.008mol/L 0.048mol/L
k=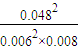 =8000,
=8000,
故答案为:0.018mol/(L?min);8000;
②第6min时,向容器中再充入0.002molO2,反应至10min时重新达到平衡,此时测得c(SO2)=0.004mol/L,等效于
2SO2+O2 2SO3
2SO3
起始:0.054mol/L 0.034mol/L 0
转化:0.050mol/L 0.025mol/L 0.050mol/L
平衡:0.004moL/L 0.009mol/L 0.050mol/L
此时k=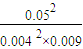 =17361>8000,说明平衡向正反应方向移动,而该反应放热,则应是降低温度,故小于500℃,
=17361>8000,说明平衡向正反应方向移动,而该反应放热,则应是降低温度,故小于500℃,
故答案为:<.
点评:本题考查无机物的推断,题目综合度较大,难度较大,易错点为(4),注意从平衡常数的角度判断平衡移动的方向.
(2)根据物质的性质书写有关反应的离子方程式并判断氧化剂和还原剂之间的关系;
(3)通入氧气的一极为原电池的正极,发生还原反应,负极发生氧化反应;
(4)①根据浓度的变化计算反应速率,根据平衡常数等于生成物浓度幂之积除以反应物浓度幂之积计算;
②计算出该温度时的平衡常数,根据温度对平衡移动的影响判断.
解答:解:(1)H和葡萄糖反应生成B为红色固体,则H为Cu(OH)2,B为Cu2O,在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,则E为酸,F为Cu,由C→D→E等反应可知,C为SO2,D为SO3,E为H2SO4,则G为CuSO4,A应含有Cu和S两种元素,质量比为4:1,应为Cu2S,故答案为:Cu2S;Cu2O;Cu(OH)2;
(2)反应Ⅰ为:2Cu2S+3O2
 2Cu2O+2SO2,由方程式可以看出,还原剂与氧化剂的物质的量之比为2:3,Cu2O在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,Cu和浓硫酸在加热条件下反应生成CuSO4和SO2,反应的化学方程式为Cu+2H2SO4(浓)
2Cu2O+2SO2,由方程式可以看出,还原剂与氧化剂的物质的量之比为2:3,Cu2O在酸性条件下反应:Cu2O+2H+=Cu+Cu2++H2O,Cu和浓硫酸在加热条件下反应生成CuSO4和SO2,反应的化学方程式为Cu+2H2SO4(浓)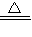 CuSO4+SO2↑+2H2O,
CuSO4+SO2↑+2H2O,故答案为:2:3;Cu2O+2H+=Cu+Cu2++H2O;Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;(3)氧气具有氧化性,应为原电池的正极,发生还原反应,二氧化硫具有还原性,应为原电池的负极,发生氧化反应,电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:正;SO2+2H2O-2e-=SO42-+4H+;
(4)①c(SO2)=
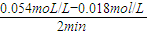 =0.018mol/(L?min),
=0.018mol/(L?min),2SO2+O2
 2SO3
2SO3起始:0.054mol/L 0.032mol/L
转化:0.048mol/L 0.024mol/L 0.048mol/L
平衡:0.006moL/L 0.008mol/L 0.048mol/L
k=
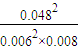 =8000,
=8000,故答案为:0.018mol/(L?min);8000;
②第6min时,向容器中再充入0.002molO2,反应至10min时重新达到平衡,此时测得c(SO2)=0.004mol/L,等效于
2SO2+O2
 2SO3
2SO3起始:0.054mol/L 0.034mol/L 0
转化:0.050mol/L 0.025mol/L 0.050mol/L
平衡:0.004moL/L 0.009mol/L 0.050mol/L
此时k=
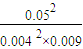 =17361>8000,说明平衡向正反应方向移动,而该反应放热,则应是降低温度,故小于500℃,
=17361>8000,说明平衡向正反应方向移动,而该反应放热,则应是降低温度,故小于500℃,故答案为:<.
点评:本题考查无机物的推断,题目综合度较大,难度较大,易错点为(4),注意从平衡常数的角度判断平衡移动的方向.

练习册系列答案
相关题目
 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2.
化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2.
 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式________________________________.
化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式________________________________. 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2.
化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2.
 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式________________________________.
化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式________________________________. 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2
化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2
 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________.
化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________.