题目内容
(1)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得如下数据:
| 序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 12 |
| ② | 22.00 | 18.00 | 11 |
| ③ | 22.00 | 22.00 | 7 |
x=________ ;Ba(OH)2溶液的物质的量浓度为________________
(2)常温下,向100mL pH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH________7(填“>”“<” 或“=”);原混合溶液中硫酸钠的物质的量浓度为________
2 , 0.005 mol·L-1 > 0.01 mol·L-1
(1)氢氧化钡中OH-的浓度是0.01mol/L,则氢氧化钡的浓度是 0.005 mol·L-1。恰好反应时,消耗盐酸是22.00m,所以盐酸的浓度为0.01mol/L,则pH=2。300ml氢氧化钡中OH-的物质的量是0.003mol,混合液中氢离子是0.001mol,所以剩余OH-的物质的量是0.002mol,溶液显碱性。混合物中硫酸是0.0005mol,消耗氢氧化钡也是0.0005mol。则和硫酸钠反应的氢氧化钡是0.005 mol·L-1 ×0.3L-0.0005mol=0.001mol,所以浓度是0.001mol÷0.1L==0.01mol/L。
(1)氢氧化钡中OH-的浓度是0.01mol/L,则氢氧化钡的浓度是 0.005 mol·L-1。恰好反应时,消耗盐酸是22.00m,所以盐酸的浓度为0.01mol/L,则pH=2。300ml氢氧化钡中OH-的物质的量是0.003mol,混合液中氢离子是0.001mol,所以剩余OH-的物质的量是0.002mol,溶液显碱性。混合物中硫酸是0.0005mol,消耗氢氧化钡也是0.0005mol。则和硫酸钠反应的氢氧化钡是0.005 mol·L-1 ×0.3L-0.0005mol=0.001mol,所以浓度是0.001mol÷0.1L==0.01mol/L。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目

 HCO3-+OH-,与油污发生反应,达到去污目的
HCO3-+OH-,与油污发生反应,达到去污目的 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: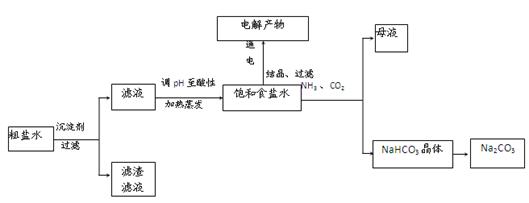
 离子,加入下列沉淀剂的顺序是(填序号) 。
离子,加入下列沉淀剂的顺序是(填序号) 。