题目内容
5.标准状况下,3.36L某无色可燃性气体A在足量的氧气中完全燃烧.若将产物通入足量的石灰水中,得到白色沉淀的质量为30.0g;若用足量的碱石灰吸收燃烧后的产物,增重18.6g.(1)计算燃烧产物中二氧化碳的质量.
(2)若原气体是单一气态烃,通过计算推断它的分子式,并写出电子式和结构简式.
分析 (1)白色沉淀30.0g为碳酸钙的质量,根据n=$\frac{m}{M}$计算碳酸钙的物质的量,根据碳原子守恒计算n(CO2),根据m=nM计算二氧化碳的质量;
(2)碱石灰增重18.6g为燃烧生成的二氧化碳与水,可以计算生成水的质量,计算水与气体A的物质的量,利用原子守恒计算该气态烃的分子式,书写其电子式及可能的结构简式.
解答 解:(1)白色沉淀30.0g为碳酸钙的质量,故碳酸钙的物质的量=$\frac{30.0g}{100g/mol}$=0.3mol,n(CO2)=n(CaCO3)=0.3mol,m(CO2)=0.3mol×44g/mol=13.2g,
答:燃烧产物中二氧化碳为13.2g;
(2)碱石灰增重18.6g为燃烧生成的二氧化碳与水,故m(H2O)=18.6g-13.2g=5.4g,则n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,则n(H)=n(H2O)×2=0.6mol,n(C)=n(CO2)=0.3mol,3.36L该气态烃的物质的量=$\frac{3.36L}{22.4L/mol}$=0.15mol,故该烃分子中N(C)=$\frac{0.3mol}{0.15mol}$=2、N(H)=$\frac{0.6mol}{0.15mol}$=4,故该烃分子式为C2H4,其电子式为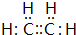 ,结构简式为CH2=CH2,
,结构简式为CH2=CH2,
答:该烃分子式为C2H4,电子式为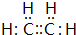 ,结构简式为CH2=CH2.
,结构简式为CH2=CH2.
点评 本题考查有机物分子式的确定,难度不大,注意掌握燃烧法利用守恒思想确定有机物分子组成方法.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
16.下列事实不能用于判断金属性相对强弱的是( )
| A. | 金属元素在金属活动顺序表中的位置 | |
| B. | 1mol金属单质在反应中失去电子数目的多少 | |
| C. | 金属元素的最高价氧化物对应的水化物的碱性强弱 | |
| D. | 金属单质与水或酸反应置换出氢气的难易程度 |
13.可逆反应3H2(g)+N2(g)?2NH3(g)△H<0,达到平衡后,为了使H2的转化率增大,下列选项中采用的三种方法都正确的是( )
| A. | 升高温度,降低压强,增加氮气 | B. | 降低温度,增大压强,加入催化剂 | ||
| C. | 升高温度,增大压强,增加氮气 | D. | 降低温度,增大压强,分离出部分氨 |
20.往溴水中加入苯后,振荡、静置,溴水层颜色变浅,这是由于( )
| A. | 溴挥发出了 | B. | 发生了取代反应 | C. | 发生了加成反应 | D. | 发生了萃取 |
10.氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.
(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图.则反应过程中放出的总热量应为234kJ.
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的 关系如下表:
①写出该反应的平衡常数表达式.K=$\frac{c{\;}^{2}(NH{\;}_{3})}{c(N{\;}_{2})×c{\;}^{3}(H{\;}_{2})}$.
②试判断K1>K2(填写“>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)=3v(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)化合物N2 H4 做火箭发动机的燃料时,与氧化剂N2O4反应生成N2和水蒸气.
某同学设计了一个N2H4--空气碱性燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图2所示.
①该燃料电池的负极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②理论上乙中两极所得气体的体积随时间变化的关系如丙图中曲线 I、II所示(气体体积已换算成标准状况下的体积),写出在t1-t2时间段铁电极上的电极反应式Cu2++2e-=Cu;原混合溶液中NaCl的物质的量浓度为0.1mol/L
③在t2时所得溶液的pH为1.(假设溶液体积不变)

(1)如图1是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图.则反应过程中放出的总热量应为234kJ.
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的 关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1>K2(填写“>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)=3v(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)化合物N2 H4 做火箭发动机的燃料时,与氧化剂N2O4反应生成N2和水蒸气.
某同学设计了一个N2H4--空气碱性燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图2所示.
①该燃料电池的负极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②理论上乙中两极所得气体的体积随时间变化的关系如丙图中曲线 I、II所示(气体体积已换算成标准状况下的体积),写出在t1-t2时间段铁电极上的电极反应式Cu2++2e-=Cu;原混合溶液中NaCl的物质的量浓度为0.1mol/L
③在t2时所得溶液的pH为1.(假设溶液体积不变)

17.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 ? NaOH H2O |
14.下列说法正确的是( )
| A. | 升高温度,正反应速率增大,逆反应速率减小 | |
| B. | 在温度和体积一定的情况下,通入氦气化学反应速率不变 | |
| C. | 增大压强可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 使用催化剂,可以改变反应的△H |
15.下列各组物质互为同素异形体的是( )
| A. | 12C和14C | B. | H2O和D2O | C. | O2和O3 | D. | 淀粉和纤维素 |