题目内容
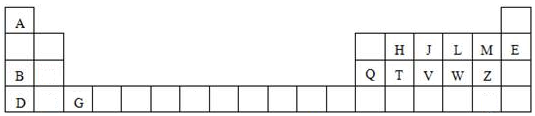
【题目】根据元素周期律判断,不正确的是
A.酸性:H3PO4>H2SO4B.稳定性:HF>HCl
C.原子半径:Na>SD.失电子能力:Ca>Mg
【答案】A
【解析】
A.S和P同周期,S的非金属性更强,所以S的最高价氧化物形成的水化物H2SO4酸性强于P对应的H3PO4,A项错误;
B.F的非金属性强于Cl,所以其简单氢化物HF相比于HCl更稳定,B项正确;
C.同周期从左至右,原子半径逐渐减小,所以Na原子的半径比S原子半径大,C项正确;
D.元素金属性越强,对应单质的失电子能力越强;同主族从上至下,金属性逐渐增强,所以Ca的失电子能力强于Mg,D项正确;
答案选A。

【题目】草酸与高锰酸钾在酸性条件下能够发生反应:MnO4+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
【实验设计】
甲组方案:通过测定生成CO2气体体积的方法来比较反应速率的大小.实验装置如图所示,25℃时将装置中的A溶液一次性加入B溶液(均已加入等量硫酸酸化)中.
实验编号 | A溶液 | B溶液 |
① | 2mL 0.1mol/LH2C2O4溶液 | 4mL0.0l1mol/L酸性KMnO4溶液 |
② | 2mL 0.2mol/LH2C2O4溶液 | 4mL0.01 mol/L酸性KMnO4溶液 |
(1)该反应中氧化剂和还原剂的物质的量之比为 .
(2)该实验探究的是对反应速率的影响.实现该实验目的还欠缺的仪器: . 比较①、②两组化学反应速率大小的方法是 .
乙组方案:用4mL0.0l1mol/L酸性KMnO4溶液与2mL 0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.具体实验如下:
实验编号 | 10%硫酸的体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | ﹣ |
Ⅱ | 2 | 20 | 少量MnSO4粉末 |
Ⅲ | 2 | 30 | ﹣ |
Ⅳ | 1 | 20 | 1mL蒸馏水 |
(3)若要研究催化剂对化学反应速率的影响,则应对比实验(填序号,下同);若要研究温度对化学反应速率的影响,则应对比实验 .
(4)对比实验I和实验Ⅳ,可以研究硫酸的浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是 .