题目内容
19.一定条件下某混合气体由两种气态烃组成.2.24L该混合气体完全燃烧后,得到4.48L二氧化碳(气体已折算成标准状况)和4.5g水.则这两种气体可能是( )| A. | CH4和C2H4 | B. | C2H4 和C5H8 | C. | C2H4 和C3H4 | D. | C2H4 和C2H6 |
分析 标准状况下2.24L该混合气体的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,完全燃烧得到4.48L二氧化碳和4.5g水,生成二氧化碳的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,水的物质的量为:$\frac{4.5g}{18g/mol}$=0.25mol,则说明混合气体平均分子式为C2H5,利用平均值法判断.
解答 解:标准状况下2.24L该混合气体的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,完全燃烧得到4.48L二氧化碳和4.5g水,生成二氧化碳的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,水的物质的量为:$\frac{4.5g}{18g/mol}$=0.25mol,则说明混合气体平均分子式为C2H5,
A.CH4和C2H4的平均C原子数小于2,平均H原子数位,不可能为C2H5,故A错误;
B.C2H4 和C5H8的平均C原子数一定大于2,不可能为C2H5,故B错误;
C.C2H4 和C3H4的平均C原子数大于2,平均H原子数为4,不可能为C2H5,故C错误;
D.C2H4 和C2H6的平均C原子数为2,平均H原子数可以为5,所以平均分子式可以为C2H5,故D正确;
故选D.
点评 本题考查混合物的计算、有机物分子式确定,注意利用平均分子式进行判断,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.

练习册系列答案
相关题目
10.下列有机物不能发生消去反应的是( )
| A. | 2-丙醇 | B. | 2,2-二甲基-1-丙醇 | ||
| C. | 2-甲基-2-丙醇 | D. | 氯乙烷 |
7.下列有关有机物分离提纯的方法正确的是( )
| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出I2 | |
| B. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶,再干燥 | |
| D. | 除去乙醇中的微量水可加入金属钠,使其完全反应 |
4.只用下列试剂中的一种就能鉴别AgNO3、Na2CO3、K2SO4三种溶液,则该试剂是( )
| A. | KNO3溶液 | B. | Na2SO4溶液 | C. | NaOH溶液 | D. | 稀HCl |
11.下列反应不属于氧化还原反应的是( )
| A. | CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 | B. | NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+HCl | ||
| C. | CuSO4+Zn=ZnSO4+Cu | D. | 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
8.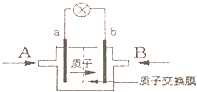 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
 一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )
一种新型的乙醇电池,它用磺酸类质子溶剂.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图,下列说法正确的是( )| A. | A处通氧气,B处通乙醇 | |
| B. | 电池工作时电子由a极沿导线经灯泡再到b极 | |
| C. | 电池正极的电极反应为:O2+2H2O+4e-=4OH- | |
| D. | 若用这种电池作电源保护金属铁,则a电极连接石墨,b连接铁 |
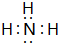 ;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.

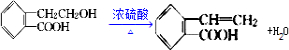 .
.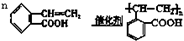 .
.