题目内容
12.下列除去杂质的方法正确的是( )| A. | 除去CO2中混有的SO2:用氢氧化钠溶液洗气 | |
| B. | 除去Cl2中混有的HCl:用饱和食盐水洗气 | |
| C. | 除去FeCl2溶液中混有的FeCl3:加入过量铜粉,过滤 | |
| D. | 除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
分析 A.二者都与氢氧化钠溶液反应;
B.氯气不溶于饱和食盐水;
C.生成氯化铜,引入新杂质;
D.二者都与硝酸反应.
解答 解:A.二者都与氢氧化钠溶液反应,应用饱和碳酸氢钠溶液除杂,故A错误;
B.氯气不溶于饱和食盐水,而氯化氢易溶于水,可用于除杂,故B正确;
C.生成氯化铜,引入新杂质,应加入铁粉除杂,故C错误;
D.二者都与硝酸反应,应用盐酸除杂,故D错误.
故选B.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意除杂时不能引入新的杂质,且不能影响被提纯物质的性质,难度不大.

练习册系列答案
相关题目
12.三位分别来自法国、美国、荷兰的科学家因研究“分子机器的设计与合成”而获得2016年诺贝尔化学奖.纳米分子机器日益受到关注,机器的“车轮”常用组件如下,下列说法正确的是( )
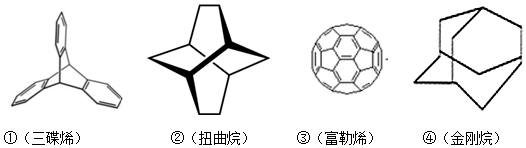

| A. | ①③均能发生加成反应 | B. | ①④互为同分异构体 | ||
| C. | ①②③④均属于烃 | D. | ①②③④的一氯代物均只有一种 |
3.设NA为阿伏伽德罗常数的数值,则下列说法正确的是( )
| A. | 等质量的CO、N2含有的分子数均为NA | |
| B. | 0.5 mol/L的MgCl2溶液中Cl-离子的物质的量为NA | |
| C. | 常温常压时,4.48 L CH4气体中含有的原子数大于NA | |
| D. | 12克13C含有的碳原子数小于NA |
20.反应A(g)+3B(g)=2C(g)+2D(g),不同情况下测得反应速率,其中反应速率最快的是( )
| A. | υ(D)=0.4 mol/(L•s) | B. | υ(C)=30 mol/(L•min) | C. | υ(B)=0.9 mol/(L•s) | D. | υ(A)=0.15 mol/(L•s) |
7.下列离子方程式书写正确的是( )
| A. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- | |
| B. | FeSO4溶液中加入酸性H2O2溶液:Fe2++2H2O2+4H+═Fe3++4H2O | |
| C. | Cl2和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2+2H2O |
17.下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | Na2CO3+H2SO4;Na2CO3+HCl | ||
| C. | CaCO3+H2SO4;CaCO3+HCl | D. | BaCl2+H2SO4;Ba(OH)2+H2SO4 |
1.对已经达到化学平衡的反应2X(g)+Y(g)?2Z(g),△H<0( )
| A. | 减小压强时,正、逆反应速率都减小,平衡向正反应方向移动 | |
| B. | 降低温度时,正、逆反应速率都减小,平衡向逆反应方向移动 | |
| C. | 恒容时,充入稀有气体,Y的转化率变大 | |
| D. | 此反应为熵减反应,△S<0 |
2.短周期元素X、Y、Z、W在元素周期表中的相对位置关系如图所示.下列判断正确的是( )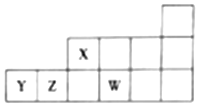

| A. | 原子半径:rW>rZ>rY>rX | |
| B. | 最高价氧化物对应水化物的酸性:Z>X>Y | |
| C. | X、Z、W形成的简单氢化物中X的氢化物沸点最高 | |
| D. | W与Y元素形成的化合物在水溶液中能稳定存在 |