题目内容
16.以下关于有机化合物的认识正确的是( )| A. | 某烷烃CnH2n+2的一个分子中,含有共价键的数目是3n+1 | |
| B. | 用HNO3酸化的AgNO3溶液检验CCl4中是否含有氯元素 | |
| C. | 红热的铜丝可以和乙醇发生置换反应产生氢气 | |
| D. | 石油化工得到的产品均为液体,煤化工得到的产品有液体也有固体 |
分析 A、烷烃是饱和链烃,烷烃的通式为CnH2n+2,碳原子间以单键连接,碳原子形成四个化学键,即碳氢单键、碳碳单键的数目和;
B、用HNO3酸化的AgNO3溶液,可检验氯离子,但是四氯化碳中不含有氯离子;
C、红热的铜丝可以和乙醇发生氧化反应生成乙醛;
D、石油产品、煤的化工产品均有气体、液体等.
解答 解:A、依据烷烃是饱和链烃,碳原子间以单键连接,碳原子形成四个化学键分析判断,烷烃的通式是:CnH2n+2,含有碳碳单键数为n-1,含有碳氢单键数为2n+2,所以形成共价键数目为n-1+2n+2=3n+1,故A正确;
B、四氯化碳中的氯元素不是氯离子,故此方法错误,故B错误;
C、红热的铜丝可以和乙醇发生氧化反应生成乙醛,不会发生置换反应生成氢气,故C错误;
D、石油产品、煤的化工产品均有气体、液体等,如含烃类物质中有气体、液体等,故D错误,故选A.
点评 本题考查较综合,涉及有机物的结构与性质、有机物反应类型、组成和性质等,综合性较强,注重基础知识的考查,选项C为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.如表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na;
(2)最高价氧化物的水化物中碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(3)A与H形成共价化合物(填“离子”或“共价”),用电子式表示它的形成过程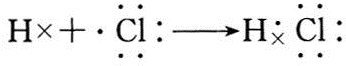 ;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程
;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程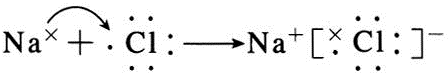 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物中碱性最强的是NaOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(3)A与H形成共价化合物(填“离子”或“共价”),用电子式表示它的形成过程
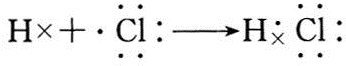 ;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程
;B与G形成离子化合物(填“离子”或“共价”),用电子式表示它的形成过程 .
.
11.一定温度下,将浓度为0.1mol•L-1的Na2CO3溶液加水不断稀释,下列各值始终增大的是( )
| A. | c(H+) | B. | c(HCO${\;}_{3}^{-}$) | ||
| C. | c(H+)•c(OH-) | D. | $\frac{c(O{H}^{-})•c(HC{{O}_{3}}^{-})}{c(C{{O}_{3}}^{2-})}$ |
8. 新型能源氢能的关键技术是储氢.如图装置可实现有机物的电化学储氢(忽略其它有机物),储氢装置的电流效率η=生成目标产物消耗的电子数/转移的电子总数×100%,则下列说法正确的是( )
新型能源氢能的关键技术是储氢.如图装置可实现有机物的电化学储氢(忽略其它有机物),储氢装置的电流效率η=生成目标产物消耗的电子数/转移的电子总数×100%,则下列说法正确的是( )
 新型能源氢能的关键技术是储氢.如图装置可实现有机物的电化学储氢(忽略其它有机物),储氢装置的电流效率η=生成目标产物消耗的电子数/转移的电子总数×100%,则下列说法正确的是( )
新型能源氢能的关键技术是储氢.如图装置可实现有机物的电化学储氢(忽略其它有机物),储氢装置的电流效率η=生成目标产物消耗的电子数/转移的电子总数×100%,则下列说法正确的是( )| A. | 该储氢装置的电流效率η=64.3% | |
| B. | D电极室发生的所有的电极反应为:C4H6+6H++6e-═C6H12 | |
| C. | B电极为电源的负极 | |
| D. | H+由D电极室移向E电极室 |
5.下列物质属于离子化合物的是( )
| A. | NaF | B. | H2O | C. | HBr | D. | CH4 |
6.已知短周期主族元素W,X,Y,Z的原子序数依次增大,W,X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )
| A. | Y,Z形成的分子空间构型可能是正四面体 | |
| B. | W,Y,Z的电负性大小顺序一定是Z>Y>W | |
| C. | WY2分子中δ键与π键的数目之比是2:1 | |
| D. | W,X,Y,Z的原子半径大小顺序可能是W>X>Y>Z |
 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①乙烯、②H乙炔、③苯、④甲醛.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键(须指明加成产物是何物质)
,很多不饱和有机物在E催化下可与H2发生加成反应:如①乙烯、②H乙炔、③苯、④甲醛.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键(须指明加成产物是何物质)

 DCH3COOOH
DCH3COOOH .
.