题目内容
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如下图所示,符合图中情况的一组物质是( )
| X | Y |
A | Ba(HCO3)2溶液 | NaOH溶液 |
B | KOH溶液 | Mg(HSO4)2溶液 |
C | Na2CO3溶液 | CaCl2溶液 |
D | CO2气体 | 石灰水 |

B
【解析】 由图可以看出,反应开始一段时间无沉淀,加入一定量的X后,沉淀达到最大值且不会溶解。Ba(HCO3)2与NaOH溶液混合即产生BaCO3沉淀,A不合题意;KOH与Mg(HSO4)2溶液混合,当KOH少量时,OH-与H+反应,生成MgSO4溶于水,无沉淀,继续加KOH,会产生Mg(OH)2沉淀,B符合题意;Na2CO3与CaCl2溶液混合即产生CaCO3沉淀,C不合题意;石灰水中通入CO2气体,当CO2气体少量时,生成CaCO3沉淀,通入过量的CO2气体,生成的CaCO3沉淀溶解,D不合题意。所以符合题意的为B。

乙二酸(H2C2O4)俗名草酸,草酸易溶于水,市售消字灵一般为高锰酸钾和草酸的混合溶液。
(1) 在KMnO4与H2C2O4反应中,可通过测定____________来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:_______________ _____________;
(2) 某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,H2C2O4水溶液可以用酸性KMnO4溶液进行滴定
该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③已知用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,逐滴加入到装有草酸溶液的锥形瓶中,到滴定终点时,停止滴定。开始时读数及恰好反应时KMnO4溶液的读数见下表。
| 实验编号 | 待测草酸溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) |
| ① | 25.00 | 0.00 | 10.00 m |
| ② | 25.00 | 1.00 | 11.02 |
| ③ | 25.00 | 0.22 | 12.00 |
请回答:滴定时,将KMnO4标准液装在 (填“酸式滴定管”或“碱式滴定管”)中。
请在下面空白处通过上述数据,计算出待测的草酸的物质的量浓度 mol/L。计算出x= 。若滴定终点时俯视滴定管刻度,则由此测得的x值会 ;若滴定后,滴定关尖嘴处有气泡,则由此测得的x值会 。填“偏大”、“偏小”或“不变”)。


 ,Y
,Y B.X
B.X ,Y
,Y
 ,YHCl
D.X
,YHCl
D.X ,YNaOH
,YNaOH

 ,Y
,Y
 ,Y
,Y
 ,YHCl
,YHCl ,YNaOH
,YNaOH

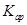 =2.5×
=2.5× 。现将该沉淀放入0.5 mol·
。现将该沉淀放入0.5 mol· 的BaCl2溶液中,其
的BaCl2溶液中,其 ________(填“增大”、“减小”或“不变”),组成不溶物F的阴离子在溶液中的浓度为________mol·
________(填“增大”、“减小”或“不变”),组成不溶物F的阴离子在溶液中的浓度为________mol·