题目内容
NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A.1mol乙烷(CH3CH3)中含有共价键的数目为6NA
B.由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA
C.标准状况下,22.4LH2O中含氢原子数为2NA
D.制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA
B
【解析】
试题分析:A、乙烷分子内含有7个共价键,所以1mol乙烷(CH3CH3)中含有共价键的数目为7NA,错误;B、CO2和O2分子都含有2个O原子,所以由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA,正确;C、H2O在标准状况下不是气态,不能用22.4L/mol进行换算,错误;D、制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为0.5NA,错误。
考点:本题考查阿伏伽德罗常数的应用。

[化学—选修3:物质结构与性质](15分)
有A、B、C、D、E、F、G、H原子序数递增的前四周期八种元素。请根据下列信息,回答问题:
①A、B、C、D、E、F为短周期主族元素,原子半径大小关系为A<D<C<B<F<E; |
②A与D形成的化合物常温下为液态; |
③B元素原子价电子(外围电子)排布为nSnnPn |
④F元素原子的核外p电子总数比s电子总数多1; |
⑤第一电子能:F<E; |
⑥G的基态原子核外有6个未成对电子; |
⑦H能形成红色(或砖红色)的 |
(1)G元素基态原子的价电子排布图为 。
(2) 中B原子采取的杂化轨道类型为 。
中B原子采取的杂化轨道类型为 。
(3)根据等电子体原理,推测 分子的空间构型为 。
分子的空间构型为 。
(4)下列有关E、F的叙述正确的是( )
a.离子半径E>F b.电负性E<F
c.单质的熔点E>F d. E、F的单质均能与氧化物发生置换
e. E的氧化物具有两性 f. E、F均能与氯元素构成离子晶体
(5) 极易溶于
极易溶于 ,原因是 。
,原因是 。
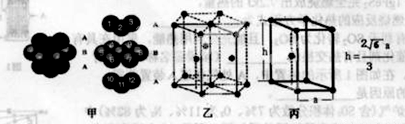
(6)E单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,晶胞如下图丙所示。则E单质的晶体堆积模型为 。
若已知E原子半径为r pm, 表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和
表示阿伏伽德罗常数,晶胞的边长为a。晶胞的高为h,则晶胞的密度可表示为 g/cm3。(用只含r和 代数式表示)
代数式表示)