题目内容
X、Y、Z和W代表原子序数依次增大的4种短周期元素.X元素原子最外层电子数比次外层电子数多2;Y与X、Z相邻,Z比Y的电子数多8;W元素原子最外层电子数等于电子层数的2倍.下列说法正确的是( )
| A、原子半径:Y>Z>W |
| B、气态氢化物的稳定性:Y>Z |
| C、W元素氧化物对应的水化物一定是强酸 |
| D、Z单质的熔沸点高于W单质 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z和W代表原子序数依次增大的4种短周期元素.X元素原子最外层电子数比次外层电子数多1,最外层电子数不大于8,则次外层只能是第一电子层,所以X是B元素;Z与Y相邻,Z比Y的电子数多8,所以Y和Z属于同一主族元素,Y原子序数大于X,所以Y属于第二周期元素,Z属于第三周期元素;W元素原子最外层电子数等于电子层数的2倍,W的最外层电子数不大于8,W原子序数大于Z,处于第三周期,所以W是S元素;通过以上分析知,Y和Z可能分别是C和Si或N和P.
解答:
解:X、Y、Z和W代表原子序数依次增大的4种短周期元素.X元素原子最外层电子数比次外层电子数多1,最外层电子数不大于8,则次外层只能是第一电子层,所以X是B元素;Z与Y相邻,Z比Y的电子数多8,所以Y和Z属于同一主族元素,Y原子序数大于X,所以Y属于第二周期元素,Z属于第三周期元素;W元素原子最外层电子数等于电子层数的2倍,W的最外层电子数不大于8,W原子序数大于Z,处于第三周期,所以W是S元素;通过以上分析知,Y和Z可能分别是C和Si或N和P,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Z>W>Y,故A错误;
B.同主族自上而下非金属性减弱,元素氢化物稳定性减弱,故氢化物稳定性Y>Z,故B正确;
C.如果Y是C元素,则Y元素最高价氧化物对应的水化物碳酸是弱酸,故C错误;
D.Z单质可能为原子晶体,W单质为分子晶体,Z单质的熔沸点可能高于W,故D错误,
故选B.
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Z>W>Y,故A错误;
B.同主族自上而下非金属性减弱,元素氢化物稳定性减弱,故氢化物稳定性Y>Z,故B正确;
C.如果Y是C元素,则Y元素最高价氧化物对应的水化物碳酸是弱酸,故C错误;
D.Z单质可能为原子晶体,W单质为分子晶体,Z单质的熔沸点可能高于W,故D错误,
故选B.
点评:本题考查原子结构与元素周期律的关系,题目侧元素周期律的递变规律的考查,注意根据原子结构特点明确元素的种类为解答该题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一定温度下的恒容容器中,当下列物理量不变时,不能表明反应:A(s)+2B(g)?C(g)+D(g)已达到平衡的是( )
| A、混合气体压强 |
| B、混合气体的密度 |
| C、混合气体的平均相对分子质量 |
| D、B的物质的量浓度 |
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.已知:B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2.由元素A、B、D组成的一元酸X为日常生活中的调味剂,元素A、F组成的化合物为Y,A与C形成的气态化合物Z在标准状况下的密度为0.76g/L,Z溶于水所得溶液为W.下列说法正确的是( )
| A、元素C在周期表中的位置是第三周期第ⅤA族 |
| B、在等体积、等pH的X、Y溶液中分别加入等质量的锌粉,充分反应后仅有一份溶液中存在锌粉,则反应过程中两溶液中反应速率的大小关系是:X<Y |
| C、由A、B、C、D四种元素形成的化合物一定只有共价键 |
| D、25℃时,将W溶液与Y溶液等体积混合,充分反应后若pH=7则c(W)>c(Y) |
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B、由X、Y和氢三种元素形成的化合物中一定只有共价键 |
| C、W、X、Z三种元素最高价氧化物对应水化物的酸性逐渐减弱 |
| D、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA |
| B、标准状况下,2.24 L水中含有水分子0.1 NA |
| C、1.12 L氯气中含有氯原子0.1 NA |
| D、32克O2所含的氧原子数目为2NA |
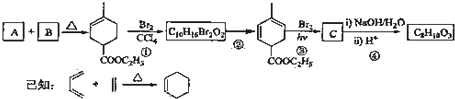
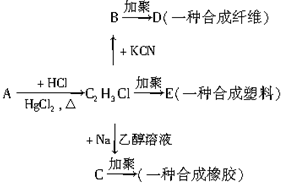 卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应:
卤代烃里的卤原子易与活泼金属阳离子结合,发生下列反应: