题目内容
钾与另一碱金属A的合金20g,与足量水反应后,放出H2 1.0g,则金属A的名称是________.
答案:锂
解析:
提示:
解析:
|
用平均值法: 因合金为碱金属组成,反应后价态均为+1价,若设其为R,平均相对原子质量为M, 则 2R+2H2O=2ROH+H2↑ 20g 1.0g 因为K的相对原子质量为39,大于20,则A的相对原子质量必小于20,所以该碱金属应为锂. |
提示:
|
此题可以有多种解法,如果选择合适的解题方法,可以简化解题过程,提高解题的速度和准确度. |

练习册系列答案
相关题目
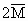 2
2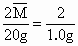 ,
,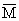 =20;
=20;