题目内容
在下列条件下,能大量共存的微粒组是
A.c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32-
B.右表提供的数据下:HClO 、HCO3-、ClO-、CO32-
C.能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I-
D.中性的溶液中:CO32-、Na+、SO42-、AlO2-
A
【解析】
试题分析:A、c(H+)=1×10-14mol/L的溶液呈碱性,各离子互不反应,可以大量共存,故A正确;B、HClO与CO32?反应生成ClO?和HCO3?,不能大量共存,故B错误;C、能与Al反应生成H2的溶液可能为酸性,也可能为碱性,酸性时,H+、NO3?能氧化I?,碱性时OH?与NH4+反应,不能大量共存,故C错误;D、CO32?、AlO2-水解使溶液呈碱性,不能在中性溶液中存在,故D错误。
考点:本题考查离子共存。

(12分)草酸与高锰酸钾在酸性条件下能够发生如下反应:
2MnO4- + 5H2C2O4 +6H+ =2Mn2+ +10CO2↑ +8H2O
用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
组别 | 10%硫酸溶液的体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2mL | 20 | 无 |
Ⅱ | 2mL | 20 | 10滴饱和MnSO4溶液 |
Ⅲ | 2mL | 30 | 无 |
Ⅳ | 1mL | 20 | 1mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,应使用实验 和 (用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,应使用实验 和 。
(2)对比实验Ⅰ和Ⅳ,可以研究 对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是 。
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
①用托盘天平称取W g Na2C2O4晶体。
②将WgNa2C2O4配成100 mL标准溶液,量取20.00 mL置于锥形瓶中,
酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中。
③若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的浓度为________ (填表达式,用W表示)。
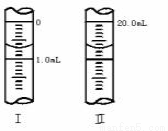
 ___________(同上)。
___________(同上)。 mol3
mol3 mol3.L-3).
mol3.L-3). H++HClO+Cl-
H++HClO+Cl- 2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)