题目内容
13.下列关于有机物的说法正确的是( )| A. | 葡萄糖与果糖、淀粉与纤维素均互为同分异构体 | |
| B. |  的同分异构体中含有苯环且属于羧酸的有14种 的同分异构体中含有苯环且属于羧酸的有14种 | |
| C. | 2,2-二甲基丙烷可以由烯烃通过加成反应制得 | |
| D. | 汽油、柴油、植物油都是碳氢化合物 |
分析 A.淀粉和纤维素的聚合度n不同,不属于同分异构体;
B. 的同分异构体中含有苯环且属于羧酸的是羧基直接与苯环连接,剩余两个碳作为乙基存在邻间对3种同分异构体,两个甲基存在6种同分异构体,若苯环连接乙酸,则存在邻间对3种同分异构体,若连接丙酸为2种;
的同分异构体中含有苯环且属于羧酸的是羧基直接与苯环连接,剩余两个碳作为乙基存在邻间对3种同分异构体,两个甲基存在6种同分异构体,若苯环连接乙酸,则存在邻间对3种同分异构体,若连接丙酸为2种;
C.2,2-二甲基丙烷,2号碳上无H原则,不能由烯烃加成;
D.仅由碳和氢两种元素组成的有机化合物称为碳氢化合物,又叫烃.
解答 解:A.葡萄糖和果糖分子式相同结构不同,属于同分异构体,淀粉和纤维素的聚合度n不同,不属于同分异构体,故A错误;
B. 的同分异构体中含有苯环且属于羧酸的是羧基直接与苯环连接,剩余两个碳作为乙基存在邻间对3种同分异构体,两个甲基存在6种同分异构体,若苯环连接乙酸,则存在邻间对3种同分异构体,若连接丙酸为2种,共14种同分异构体,故B正确;
的同分异构体中含有苯环且属于羧酸的是羧基直接与苯环连接,剩余两个碳作为乙基存在邻间对3种同分异构体,两个甲基存在6种同分异构体,若苯环连接乙酸,则存在邻间对3种同分异构体,若连接丙酸为2种,共14种同分异构体,故B正确;
C.2,2-二甲基丙烷,2号碳上无H原则,不能由烯烃加成,故C错误;
D.植物油是油脂含有氧元素不是碳氢化合物,故D错误.
故选B.
点评 本题考查了有机物性质、结构分析、同分异构体判断和书写,掌握基础是解题关键,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
3.将等体积的0.1mol/LAgNO3溶液和0.1mol/LNaCl溶液混合得到浊液,过滤后进行如下实验:

下列分析不正确的是( )

下列分析不正确的是( )
| A. | ①的现象说明上层清液中不含Ag+ | |
| B. | ②的现象说明该温度下Ag2S比Ag2SO4更难溶 | |
| C. | ③中生成Ag(NH3)2+,促进AgCl(s)溶解平衡正向移动 | |
| D. | 若向③中滴加一定量的硝酸,也可以出现白色沉淀 |
1.下列既能发生氧化还原反应,又能发生复分解反应的离子组是( )
| A. | Na+、H+、ClO-、S2- | B. | NH4+、Na+、MnO4-、I- | ||
| C. | K+、Ba2+、Br-、NO3- | D. | Mg2+、Ag+、OH-、PO43- |
8.反应N2+3H2?2NH3在密闭容器内进行.分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为v(N2)、v(H2)、v(NH3),则三者的关系正确的是( )
| A. | v(N2)=v(NH3) | B. | 3v(H2)=2v(NH3) | C. | v(NH3)=$\frac{3}{2}$v(H2) | D. | v(H2)=3v(N2) |
18.下列有关电解质溶液中粒子浓度关系正确的是( )
| A. | 将 HCl 与 CH3COONa 两溶液混合后,溶液呈中性,则 c(Na+ )<c(Cl- ) | |
| B. | 向 NH4Cl 溶液中通 NH3,则 c(NH4+ )>c(Cl- )>c(OH- )>c(H+ ) | |
| C. | 室温下,c(NH4+ )相同的①(NH4)2 CO3②(NH4)2 SO4 ③(NH4)2 Fe(SO4)2溶液浓度大小顺序为:①>②>③ | |
| D. | 已知 pKa=-lgKa,pKa(HF)=3.1,pKa(C6H5COOH)=4.2,室温下,等体积、等浓度的 NaF、C6H5COONa 溶液中,前者离子总数小于后者 |
5.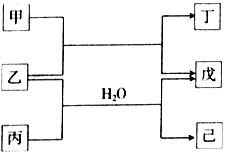 短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
 短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )| A. | 原子半径的大小Z>Y>X>R>E | |
| B. | X、Y、Z的最高价氧化物对应的水化物能相互反应 | |
| C. | E、R、Z三种元素不可能存在于同一种共价化合物中 | |
| D. | Z的阴离子夺取质子的能力较R的阴离子强 |
2.下列鉴别物质的方法能达到目的是( )
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用KSCN溶液鉴别FeCl3溶液和FeCl2溶液 | |
| D. | 用淀粉溶液鉴别加碘盐和未加碘盐(己知加碘盐中添加的是KIO3) |
7.某有机物的分子式为C9H10O2,其属于芳香族化合物且能与Na2CO3反应产生气体的同分异构体有(不考虑、立体异构)( )
| A. | 15种 | B. | 14种 | C. | 13 种 | D. | 12种 |