题目内容
由铝和某种金属组成的混合物,将它分成质量相等的两份。一份放入过量的盐酸中,混合物全部作用完,放出H2 6.16 L(标准状况),溶液质量比反应前增加4.85 g;另一份放入过量烧碱溶液中,反应完毕后,放出H2 4.48 L(标准状况),溶液的质量比反应前增加3.2 g,而某金属则不反应,沉积出来。求:(1)原混合物中某金属的质量。
(2)某金属的相对原子质量。
(1)3.6 g(2)24
解析:
(1)某金属与盐酸产生的H2为:![]() mol。
mol。
该金属与盐酸反应使溶液增重为:
4.85 g-3.2 g=1.65 g。
m(金属)=1.65 g+0.075 mol×2 g·mol-1=1.8 g,
原混合物中该金属为3.6 g。
(2)设该金属化合价为+n。
则M(金属)=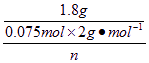 =12n
=12n
讨论n=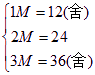

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目