题目内容
常温下,下列关于电解质溶液的判断正确的是( )
| A、在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存 |
| B、在pH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存 |
| C、0.1mol/L一元碱BOH溶液的pH=10,可推知BOH溶液中存在BOH=B++OH- |
| D、在0.1mol/L一元酸HA溶液的pH=3,可推知NaA溶液中存在:A-+H2O?HA+OH- |
考点:离子共存问题,弱电解质在水溶液中的电离平衡,盐类水解的原理
专题:
分析:A.pH=12的溶液呈碱性,离子之间不反应且和氢氧根离子不反应的能大量共存;
B.pH=0的溶液呈酸性,离子之间不反应且和氢离子不反应的能大量共存;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐.
B.pH=0的溶液呈酸性,离子之间不反应且和氢离子不反应的能大量共存;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐.
解答:
解:A.pH=12的溶液呈碱性,OH-、HCO3-反应而不能大量共存,故A错误;
B.pH=0的溶液呈酸性,NO3-、SO32-、H+发生氧化还原反应而不能大量共存,故B错误;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱,则BOH溶液中存在BOH?B++OH-,故C错误;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐,水解呈碱性,水解方程式为A-+H2O?HA+OH-,故D正确;
故选D.
B.pH=0的溶液呈酸性,NO3-、SO32-、H+发生氧化还原反应而不能大量共存,故B错误;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱,则BOH溶液中存在BOH?B++OH-,故C错误;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐,水解呈碱性,水解方程式为A-+H2O?HA+OH-,故D正确;
故选D.
点评:本题考查离子共存、弱电解质的电离、盐类水解等知识点,侧重考查氧化还原反应、复分解反应、弱电解质等知识点,明确物质或离子性质即可解答,易错选项是B.

练习册系列答案
相关题目
已知维素生A的结构简式如下,关于它的正确说法是( )


| A、维生素A是一种酚 |
| B、维生素A的一个分子中有30个氢原子 |
| C、维生素A的一个分子中有6个不饱和碳原子 |
| D、维生素A分子中处于四面体中心的碳原子有9个 |
下列物质中,不能发生消去反应的是( )
A、 |
| B、CH2 CH2Br2 |
C、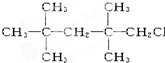 |
| D、CH2ClCH2CH3 |
下列说法正确的是( )
①漂白粉的有效成分是氯化钙和次氯酸钙②pH在5.6~7.0之间的雨水通常称为酸雨③使用二氧化硫增白的食品对人体健康产生损害④使用氯气对自来水消毒可能生成对人体有害的有机氯化物.
①漂白粉的有效成分是氯化钙和次氯酸钙②pH在5.6~7.0之间的雨水通常称为酸雨③使用二氧化硫增白的食品对人体健康产生损害④使用氯气对自来水消毒可能生成对人体有害的有机氯化物.
| A、①②③ | B、③④ |
| C、①③④ | D、①②④ |
下列反应达到平衡后降温或增压,平衡都向正反应方向移动的是( )
| A、2NH3(g)?3H2(g)+N2(g);△H>0 |
| B、3O2(g)?2O3(g);△H>0 |
| C、H2(g)+I2(g)?2HI(g);△H<0 |
| D、2NO2(g)?N2O4(g);△H<0 |
如图所示,a、b都是惰性电极,通电一段时间后,b极附近溶液显红色,下列说法中正确的是( )

| A、X是正极,Y是负极 |
| B、X是负极,Y是正极 |
| C、CuSO4溶液的pH逐渐增大 |
| D、CuSO4溶液的pH保持不变 |
关于原电池的叙述正确的是( )
| A、构成原电池的正极和负极必须是两种不同金属 |
| B、原电池是把化学能转变为电能的装置 |
| C、在铅、银和盐酸构成的原电池工作时,铅板上有5.18g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D、原电池工作时,正极和负极上发生的都是氧化还原反应 |
下列各组中的性质比较中,不正确的是( )
| A、酸性 HClO4>HBrO4>HIO4 |
| B、碱性Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C、还原性 F->Cl->Br- |
| D、稳定性 HCl>H2S>PH3 |

 ,请写出与其同类的另外两种有机物的结构简式:
,请写出与其同类的另外两种有机物的结构简式: