��Ŀ����
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á� ��ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�

��1������ȼ�ϵ�ص�����ת����Ҫ��ʽ�� __________________���ڵ����е�����������Ϊ_________ ����a��b��ʾ����
��2��������ӦʽΪ_________________ ��
��3���缫����Ʋ��۵�ԭ��Ϊ________________________��
��4���õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܡ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
��2��������ӦʽΪ_________________ ��
��3���缫����Ʋ��۵�ԭ��Ϊ________________________��
��4���õ�ع���ʱ��H2��O2�������ⲿ��������ؿ����������ṩ���ܡ���ˣ�������ȫ�����ǹؼ�����֮һ���������һ����Ҫ�Ĵ�����ϣ�����ͷ���ԭ�����£�
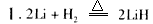
 ��
���ٷ�ӦI�еĻ�ԭ����__________ ����Ӧ���е���������______________________��
����֪LiH�����ܶ�Ϊ0.82 g/cm3���������224 L����״����H2�����ɵ�LiH����뱻���յ�H2�����Ϊ_________________________��
���ɢ����ɵ�LiH��H2O���ã��ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊ______________________ mol��
����֪LiH�����ܶ�Ϊ0.82 g/cm3���������224 L����״����H2�����ɵ�LiH����뱻���յ�H2�����Ϊ_________________________��
���ɢ����ɵ�LiH��H2O���ã��ų���H2�������ȼ�ϣ�������ת����Ϊ80%��������ͨ�����ӵ����ʵ���Ϊ______________________ mol��
��1���ɻ�ѧ��ת��Ϊ���ܣ���a��b
��2��2H2 +4OH- -4e-===4H2O��H2 +2OH- - 2e- === 2H2O
��3������缫��λ�������H2��O2���������ӿ�缫��Ӧ����
��4����Li ��H2O ��1/1148��8.71��10-4 ����32
��2��2H2 +4OH- -4e-===4H2O��H2 +2OH- - 2e- === 2H2O
��3������缫��λ�������H2��O2���������ӿ�缫��Ӧ����
��4����Li ��H2O ��1/1148��8.71��10-4 ����32

��ϰ��ϵ�д�
�����Ŀ
 AgOH+H+
AgOH+H+
 ���ϵĹ������R���Բ���
���ϵĹ������R���Բ���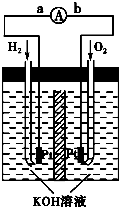 ����Ϊ
����Ϊ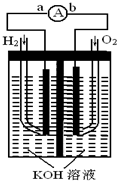 ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش� ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
 ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������� ����װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ���������� ����ǿ�������ȶ�����ش�
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������� ����װ�ã���ͼΪ���ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ���������� ����ǿ�������ȶ�����ش�