题目内容
下图表示的反应关系中,部分产物被略去,已知2 mol白色固体粉末X受热分解,恢复到室温生成A(白色固体)、B、C各1 mol,X、E、G的焰色反应均为黄色。
回答下列问题:
(1)写出下列物质的化学式:X_________,G_________,D_________;
(2)写出G与C反应生成D的离子方程式:__________________;
(3)写出X+E![]() A的离子方程式:_______________________;
A的离子方程式:_______________________;
(4)写出C与Na2O2反应的化学方程式:________________;若有0.2 mol Na2O2参加反应,则转移的电子数为________________。
(1)X:NaHCO3 G:NaAlO2 D:Al(OH)3
(2)CO2+3H2O+2![]()
![]() 2Al(OH)3↓+
2Al(OH)3↓+![]() 或是
或是![]() +CO2+2H2O
+CO2+2H2O![]() Al(OH)3↓+
Al(OH)3↓+![]()
(3)![]() +OH-
+OH-![]()
![]() +H2O
+H2O
(4)2CO2+2Na2O2![]() 2Na2CO3+O2 0.2NA或1.204×1023
2Na2CO3+O2 0.2NA或1.204×1023
解析:根据题意,“X、E、G的焰色反应均为黄色”,证明含有Na+;B、C均能与Na2O2反应生成E、A,考虑B、C可能为CO2和H2O,而E、A可能是Na2CO3和NaOH;从E+Al![]() G,可知E应是NaOH,G是NaAlO2,则B为H2O,C为CO2,A就是Na2CO3,综合以上推断可知
G,可知E应是NaOH,G是NaAlO2,则B为H2O,C为CO2,A就是Na2CO3,综合以上推断可知
(1)X:NaHCO3,G:NaAlO2,D:Al(OH)3.
(2)CO2通入NaAlO2溶液有两种反应情况,
若CO2少量则生成产物![]() ,方程式为CO2+3H2O+2
,方程式为CO2+3H2O+2![]()
![]() 2Al(OH)3↓+
2Al(OH)3↓+![]() ,
,
若CO2过量则生成产物![]() ,方程式为
,方程式为![]() +CO2+2H2O
+CO2+2H2O![]() Al(OH)3↓+
Al(OH)3↓+![]() .
.
(3)NaHCO3与NaOH反应的离子方程式为![]() +OH-
+OH-![]()
![]() +H2O.
+H2O.
(4)CO2与Na2O2反应的化学方程式为2CO2+2Na2O2![]() 2Na2CO3+O2,其中Na2O2中O元素的化合价从-1既升高到0,又降低到-2,关系式为Na2O2—e-,则有0.2 mol Na2O2参加反应,转移的电子数为0.2NA或1.204×1023.
2Na2CO3+O2,其中Na2O2中O元素的化合价从-1既升高到0,又降低到-2,关系式为Na2O2—e-,则有0.2 mol Na2O2参加反应,转移的电子数为0.2NA或1.204×1023.

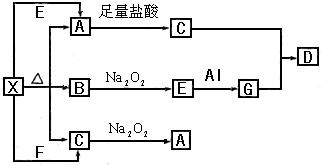 下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A.无色液体B.无色气体C各1mol.X.E.G的焰色反应均为黄色.
下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A.无色液体B.无色气体C各1mol.X.E.G的焰色反应均为黄色.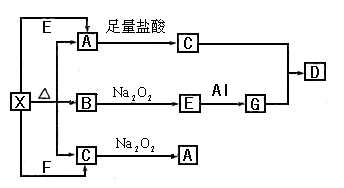
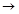 A的离子方程式:
A的离子方程式:
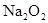 参加反应的化学方程式______________________________________,若0.2mol
参加反应的化学方程式______________________________________,若0.2mol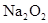 参加反应,则转移的电子数为_____________个。
参加反应,则转移的电子数为_____________个。
 A的离子方程式:_____________ ________________________
A的离子方程式:_____________ ________________________ 参加反应的化学方程式______________________________________,
参加反应的化学方程式______________________________________,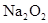 转移的电子数为_____________个。
转移的电子数为_____________个。